Buckminsterfullerène
| Buckminsterfullerène | |
| |
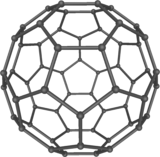
| Buckminsterfullerène C60 | |
| Identification | |
|---|---|
| Nom UICPA | (C60-Ih)[5,6]fullerène |
| Synonymes |
C60, [60]fullerène |
| No CAS | |
| No ECHA | 100.156.884 |
| PubChem | 123591 |
| ChEBI | 33128 |
| SMILES | |
| InChI | |
| Apparence | aiguilles cristallines noires |
| Propriétés chimiques | |
| Formule | C60 [Isomères] |
| Masse molaire[3] | 720,642 ± 0,048 g/mol C 100 %, |
| Diamètre moléculaire | 1,002 nm [1] (diamètre interne : 0,348 nm [2]) |
| Propriétés physiques | |
| T° fusion | >280 °C[4] sublimation à ~ 600 °C[5] |
| Solubilité | insoluble dans l'eau[4] |
| Masse volumique | 1,65 g·cm-3 [4] |
| Pression de vapeur saturante | 0,018 62 mmHg (569,85 °C)[4] |
| Cristallographie | |
| Système cristallin | cubique face centré |
| Classe cristalline ou groupe d’espace | (no 225) [6] |
| Paramètres de maille | = = = 14,041 Å α = β = γ = 90,00 ° |
| Volume | 2 768,18 Å3 [6] |
| Précautions | |
| SGH[7] | |
| H319, H335, P261, P305, P338 et P351 |
|
| NFPA 704[4] | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le buckminsterfullerène ou fullerène de Buckminster[8], parfois également appelé footballène est une molécule sphérique en C60 de la famille des fullerènes C2n, structures fermées composées de (2n-20)/2 hexagones et de 12 pentagones. C'est la plus petite du groupe, dont les atomes sont aux sommets d'un icosaèdre tronqué, i.e. forment la même structure qu'un ballon de football. C'est également le fullerène le plus fréquent.
Histoire
Découvert en 1985 par Harold Kroto, Robert Curl et Richard Smalley prix Nobel de chimie en 1996, il est nommé ainsi en l'honneur de Richard Buckminster Fuller, architecte américain, inventeur du dôme géodésique.
Structure
Le buckminsterfullerène a une structure fermée composée de 20 hexagones et 12 pentagones, aux sommets desquels se trouvent les atomes de carbone. Chaque pentagone est entouré de cinq hexagones.
Le groupe de symétrie ponctuelle du C60 est 53m en notation de Hermann-Mauguin (Ih en notation de Schoenflies) : tous les atomes de carbone occupent des sites équivalents.
Les liaisons covalentes doubles 6:6 (entre deux hexagones) sont plus courtes que les liaisons simples 6:5 (entre un hexagone et un pentagone) : 0,140 nm pour les liaisons 6:6 et 0,146 nm pour les liaisons 5:6[9].
Applications
Cette molécule est très utilisée en chimie supramoléculaire[10] et dans le domaine des nanotechnologies, en particulier comme roues dans la fabrication de nanomachines (nanovoitures, nanodragsters, etc.)[11].
Le C60 a aussi la propriété rare et remarquable de former, avec le tétrakis(diméthylamino)éthylène, un aimant purement organique en dessous de 16,1 K[12].
Anecdotiquement, il est possible de manipuler le buckminsterfullerène afin de créer un matériau plus dur que le diamant[13]. Cela devra toutefois être confirmé par d'autres expériences indépendantes.
Références
- (en) H. Tanaka et K. Takeuchi, « Diameter determination of C60 and C70 monomers in the gas phase using a differential mobility analyzer », Applied Physics A: Materials Science & Processing, Springer Berlin / Heidelberg, vol. 80, no 4, , p. 759-761 (ISSN 0947-8396 et 1432-0630, DOI 10.1007/s00339-004-2946-x)
- (en) « Physical Properties of Fullerenes », sur sesres.com (consulté le )
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Carbon (fullerene-C60) », sur ull.chemistry.uakron.edu (consulté le )
- Eiji Ōsawa, Perspectives of fullerene nanotechnology, 2002, Springer, p. 275. (ISBN 978-0-7923-7174-8), Googlebook, consulté le 26 décembre 2011.
- (en) « Fullerene C60 », sur www.reciprocalnet.org (consulté le )
- SIGMA-ALDRICH
- [PDF] « buckminsterfullerène », sur Vocabulaire panlatin de la nanotechnologie.
- (en) K. Hedberg, L. Hedberg, D.S. Bethune, C.A. Brown, H.C. Dorn, R.D. Johnson et M. de Vries, « Bond Lengths in Free Molecules of Buckminsterfullerene, C60, from Gas-Phase Electron Diffraction », Science, vol. 254, no 5030, , p. 410-412 (DOI 10.1126/science.254.5030.410)
- (en) N. Martin et J.-F. Nierengarten, Supramolecular chemistry of fullerenes and carbon nanotubes, Wiley, (présentation en ligne)
- (en) Guillaume Vives, JungHo Kang, Kevin F. Kelly et James M. Tour, « Molecular Machinery: Synthesis of a “Nanodragster” », Org. Lett., vol. 11, no 24, , p. 5602–5605 (DOI 10.1021/ol902312m)
- (en) Pierre-Marc Allemand, Kishan C. Khemani, Andrew Koch, Fred Wudl, Karoly Holczer, Steven Donovan, George Grüner et Joe D. Thompson, « Organic Molecular Soft Ferromagnetism in a Fullerene C60 », Science, vol. 253, no 5017, , p. 301-302 (DOI 10.1126/science.253.5017.301)
- « Nouvelle sur le site Futura-Sciences du 22 août 2012 », sur Futura-Sciences, (consulté le )
Voir aussi
Articles connexes
Bibliographie
- Sources bibliographiques, avec Google scholar
- (en) N. S. Sariciftci & al; , Semiconducting polymer-buckminsterfullerene heterojunctions: Diodes, hotodiodes, and photovoltaic cells, - Applied Physics …, 1993








