Germanium(II)-fluorid
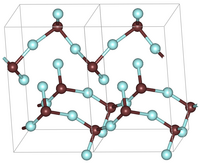
| Kristallstruktur | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||
| _ Ge2+ _ F− | ||||||||||
| Kristallsystem |
orthorhombisch | |||||||||
| Raumgruppe |
P212121 (Nr. 19) | |||||||||
| Gitterparameter |
a = 4,682 Å, b = 5,178 Å, c = 8,312 Å | |||||||||
| Allgemeines | ||||||||||
| Name | Germanium(II)-fluorid | |||||||||
| Andere Namen |
Germaniumdifluorid | |||||||||
| Verhältnisformel | GeF2 | |||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 110,64 g·mol−1 | |||||||||
| Aggregatzustand |
fest[1] | |||||||||
| Schmelzpunkt | ||||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Germanium(II)-fluorid (GeF2) ist eine anorganische chemische Verbindung des Germaniums aus der Gruppe der Fluoride.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Germanium(II)-fluorid kann durch Reaktion von Germanium(IV)-fluorid mit Germanium bei 150 °C gewonnen werden.[1]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Germanium(II)-fluorid ist ein weißer Feststoff, der löslich in 48%er Flusssäure ist. Er kann bei 130 °C im Vakuum destilliert werden und zersetzt sich oberhalb 160 °C unter Verfärbung. Er besitzt stark reduzierende Eigenschaften.[1] In feuchter Luft erfolgt Umwandlung zu Germanium(II)-hydroxid.[3] Germanium(II)-fluorid besitzt eine orthorhombische Kristallstruktur mit der Raumgruppe P212121 (Raumgruppen-Nr. 19) und den Gitterkonstanten a = 0,4682 nm, b = 0,5178 nm, c = 0,8312 nm sowie vier Formeleinheiten pro Elementarzelle. Seine Kristallstruktur besteht aus starken Polymerketten, die aus GeF3-Pyramiden bestehen, wobei eines der Fluoratome in der Kette zu zwei benachbarten Pyramiden gehört.[4]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 230.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. Taylor & Francis US, 2011, ISBN 1-4398-1462-7, S. 187 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ James Trotter, M. Akhtar, Neil Bartlett: The crystal structure of germanium difluoride. In: Journal of the Chemical Society A: Inorganic, Physical, Theoretical. 1966, S. 30, doi:10.1039/J19660000030.
