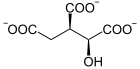
Isocitrat-Dehydrogenase

Isocitrat-Dehydrogenase (IDH) ist der Name für Enzyme und Enzymkomplexe, die die oxidative Abspaltung von Kohlenstoffdioxid von Isocitrat katalysieren, wobei α-Ketoglutarat entsteht. Diese Reaktion ist Teil des Citratzyklus und daher zentral im Stoffwechsel aller Lebewesen. Die Umkehrreaktion, die nur in manchen Mikroorganismen vorkommt, benutzt das Enzym Isocitrat-Lyase. IDH-Mutationen sind mit manchen Krebserkrankungen assoziiert.
Struktur
[Bearbeiten | Quelltext bearbeiten]Strukturell bestehen IDH aus abwechselnden α-Layern und β-Sheets in einer Sandwich-Anordnung. Es gibt zwei verschiedene Enzymgruppen, je nachdem ob NAD+ (EC 1.1.1.41) oder NADP+ (EC 1.1.1.42) Kofaktor ist. Beide haben Mg2+ oder Mn2+ als Metallion. Homologe der ersten Gruppe bestehen aus drei Untereinheiten (Heterotetramer ααβγ) und sind im Mitochondrium lokalisiert, während die zweite Gruppe Homodimere sind, mit je einer Isoform im Mitochondrium und im Cytosol.[1] IDH kommen in allen Lebewesen vor. Beim Menschen sind die drei IDH-Isoformen in fünf Genen codiert, deren Defekte zu erblichen Stoffwechselstörungen führen können:
| Gen | Protein | Aminosäuren | UniProt | OMIM | Kommentar |
|---|---|---|---|---|---|
| IDH1 | IDH(NADP), zytoplasmisch | 414 | O75874 | 147700 | Gliome |
| IDH2 | IDH(NADP), mitochondriell | 413 | P48735 | 147650 | Gliome, 2-Hydroxyglutarazidurie[2] |
| IDH3A | IDH(NAD), mitochondriell, Untereinheit alpha | 339 | P50213 | 601149 | |
| IDH3B | IDH(NAD), mitochondriell, Untereinheit beta | 351 | O43837 | 604526 | Retinitis pigmentosa[3] |
| IDH3G | IDH(NAD), mitochondriell, Untereinheit gamma | 354 | P51553 | 147700 |
Reaktionsmechanismus
[Bearbeiten | Quelltext bearbeiten]
Die im ersten Schritt erfolgende Oxidation des Isocitrats 1 liefert neben NADH die 2-Oxocarbonsäure Oxalsuccinat 2, welche als zweizähniger Ligand über die Ketogruppe und die dazu alpha-ständige Carboxygruppe das Metallion (Mn2+ oder Mg2+) komplexiert. Dadurch bedingt wird die Carbonylfunktion polarisiert, was die Neigung der betaständigen Carboxygruppe zur Decarboxylierung immens erhöht, so dass sich im nun folgenden Decarboxylierungsschritt die über die Komplexbildung stabilisierte Enolform des 2-Oxoglutarats 3 bildet. Nach Protonierung wird das 2-Oxoglutarat(α-Ketoglutarat) 4 freigesetzt. Die mitochondriale NAD+-abhängige Isocitrat-Dehydrogenase kann im Gegensatz zur NADP+-abhängigen kein Oxalsuccinat als Substrat binden, um 2-Oxoglutarat zu bilden.
Die katalysierte Reaktion:
Von Isocitrat wird CO2 abgespalten und Ketoglutarat bildet sich.
Wie jede Dehydrogenase ist auch die Isocitrat-Dehydrogenase durch ATP bzw. ADP regulierbar. Das ATP bewirkt eine indirekte Hemmung, das ADP eine indirekte Aktivierung der Dehydrogenase, da sie auf die Kinase-Untereinheit einwirken. ATP stimuliert die Kinase-Untereinheit, diese phosphoryliert die Untereinheit I der Isocitrat-Dehydrogenase, was deren Inaktivierung nach sich zieht. Entsprechend wirkt ADP als Antagonist und führt zu einer indirekten Aktivierung der Isocitrat-Dehydrogenase. Diesen Regulierungsprozess durch Phosphorylierung und Dephosphorylierung bezeichnet man als Interkonversion.
Mutationen
[Bearbeiten | Quelltext bearbeiten]IDH-Mutationen spielen bei manchen Tumorerkrankungen eine Rolle, sie sind in 80 % der Gliome und Chondrosarkome und in 20 % der akuten myeloischen Leukämien und Gallengangskarzinome zu finden. Am häufigsten sind ein Austausch der Aminosäure Arginin (R) an Position 132 von IDH1 (IDH1-R132), IDH2-R140 und IDH-R172. Fast immer ist nur eine der beiden Genkopien betroffen (Heterozygotie), insbesondere bei Rezidiven kann jedoch auch eine homzygote Mutation vorliegen.[4]
Durch die Mutation wird das Enzym so verändert, dass es unter NADPH-Verbrauch α-Ketoglutarat zum chemisch ähnlichen 2-Hydroxyglutarat umwandelt.[4] Dieser Onkometabolit führt durch kompetitive Hemmung von α-Ketoglutarat-abhängigen Dioxygenasen zu einer Hypermethylierung von Histonen (vor allem H3) und DNA (vor allem an CpG-Inseln).[5] Diese Veränderungen begünstigen die Entstehung von Tumoren, wobei die genauen Mechanismen noch unzureichend verstanden sind.[4][6] Durch den Verbrauch von NADPH steht dieses nicht mehr als Reduktionspartner für diverse Stoffwechselwege zur Verfügung, die Zelle erfährt Oxidativen Stress.[5] Tumorzellen mit IDH-Mutationen weisen folglich Defizite in der DNA-Reparatur und dem intrazellulären Transport auf, neigen zu Entzündungsprozessen und sterben vermehrt ab. Tumoren mit IDH-Mutation weisen deswegen häufig eine bessere Prognose als Vergleichbare mit IDH-Wildtyp auf.[4]
Der Wirkstoff Ivosidenib hat in der EU für die Behandlung der akuten myeloischen Leukämie und des Gallengangskarzinoms mit IHD1-Mutation einen Orphan-Arzneimittel-Status.[7] Weitere Wirkstoffe sind in anderen Regionen bereits zugelassen, beispielsweise Enasidenib bei IDH2-Mutationen, oder Gegenstand klinischer Studien.[4]
Literatur
[Bearbeiten | Quelltext bearbeiten]- P. T. Tan, A. H. Wei: The epigenomics revolution in myelodysplasia: a clinico-pathological perspective. In: Pathology, Band 43, Nummer 6, Oktober 2011, S. 536–546, doi:10.1097/PAT.0b013e32834a4061. PMID 21881538. (Review).
- L. Dang, S. Jin, S. M. Su: IDH mutations in glioma and acute myeloid leukemia. In: Trends in Molecular Medicine, Band 16, Nummer 9, September 2010, S. 387–397, doi:10.1016/j.molmed.2010.07.002. PMID 20692206. (Review).
- M. Rossetto, P. Ciccarino u. a.: Metabolism of glioma and IDH1/IDH2 mutations. In: Revue neurologique, Band 167, Nummer 10, Oktober 2011, S. 699–703, doi:10.1016/j.neurol.2011.08.002. PMID 21885076. (Review).
- A. Nekrutenko, D. M. Hillis u. a.: Cytosolic isocitrate dehydrogenase in humans, mice, and voles and phylogenetic analysis of the enzyme family. In: Molecular biology and evolution, Band 15, Nummer 12, Dezember 1998, S. 1674–1684, PMID 9866202.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ InterPro: IPR004434 Isocitrate dehydrogenase NAD-dependent (englisch)
- ↑ Eintrag zu 2-Hydroxy-Glutarazidurie. In: Orphanet (Datenbank für seltene Krankheiten)
- ↑ D. T. Hartong, M. Dange u. a.: Insights from retinitis pigmentosa into the roles of isocitrate dehydrogenases in the Krebs cycle. In: Nature genetics. Band 40, Nummer 10, Oktober 2008, S. 1230–1234, doi:10.1038/ng.223. PMID 18806796. PMC 2596605 (freier Volltext).
- ↑ a b c d e Christopher J. Pirozzi, Hai Yan: The implications of IDH mutations for cancer development and therapy. In: Nature Reviews Clinical Oncology. Band 18, Nr. 10, Oktober 2021, ISSN 1759-4774, S. 645–661, doi:10.1038/s41571-021-00521-0.
- ↑ a b Petr Ježek: 2-Hydroxyglutarate in Cancer Cells. In: Antioxidants & Redox Signaling. Band 33, Nr. 13, 1. November 2020, ISSN 1523-0864, S. 903–926, doi:10.1089/ars.2019.7902, PMID 31847543, PMC 7533892 (freier Volltext).
- ↑ Fu-Ju Chou, Yang Liu, Fengchao Lang, Chunzhang Yang: D-2-Hydroxyglutarate in Glioma Biology. In: Cells. Band 10, Nr. 9, 7. September 2021, ISSN 2073-4409, S. 2345, doi:10.3390/cells10092345, PMID 34571995, PMC 8464856 (freier Volltext).
- ↑ Tibsovo | European Medicines Agency. In: Europäische Arzneimittel-Agentur. Abgerufen am 14. Februar 2024.