Tétrachlorométhane
| Tétrachlorométhane | |
  Formule développée et représentation 3D du tétrachlorométhane |
|
| Identification | |
|---|---|
| Nom UICPA | tétrachlorométhane |
| Synonymes |
tétrachlorure de carbone |
| No CAS | |
| No ECHA | 100.000.239 |
| No CE | 200-262-8 |
| PubChem | 5943 |
| ChEBI | 27385 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore, d'odeur caractéristique[1]. |
| Propriétés chimiques | |
| Formule | CCl4 [Isomères] |
| Masse molaire[3] | 153,823 ± 0,009 g/mol C 7,81 %, Cl 92,19 %, |
| Diamètre moléculaire | 0,537 nm[2] |
| Propriétés physiques | |
| T° fusion | −23 °C[4] |
| T° ébullition | 76,7 °C[4] |
| Solubilité | 800 mg·l-1 dans l'eau à 20 °C[4] |
| Paramètre de solubilité δ | 17,6 MPa1/2 (25 °C)[5] |
| Masse volumique | 1,594 liquide 1.831 à −186 °C (solide) 1.809 à −80 °C (solide) 5.32 (/ air) |
| T° d'auto-inflammation | 982 °C[4] |
| Pression de vapeur saturante | 119,4 hPa (20 °C) 186,1 hPa (30 °C) |
| Point critique | 45,6 bar, 283,25 °C[7] |
| Vitesse du son | 930 m·s-1 à 25 °C [8] |
| Thermochimie | |
| S0gaz, 1 bar | 309,41 J·K-1·mol-1 |
| S0liquide, 1 bar | 214,43 J·K-1·mol-1 |
| ΔfH0gaz | −106,69 kJ·mol-1 |
| ΔfH0liquide | −139,49 kJ·mol-1 |
| Cp | 83,51 J·K-1·mol-1 (g) 131,75 J·K-1·mol-1 (l) |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 11,47 ± 0,01 eV (gaz)[10] |
| Cristallographie | |
| Paramètres de maille | a = 9,079 Å b = 5,764 Å |
| Volume | 466,60 Å3[11] |
| Propriétés optiques | |
| Indice de réfraction | 1,457[2] |
| Précautions | |
| SGH[14] | |
| H301, H311, H331, H351, H372, H412 et EUH059 |
|
| SIMDUT[15] | |
 D1A, D2A, D2B, |
|
| NFPA 704 | |
| Transport | |
| Classification du CIRC | |
| Groupe 2B : Peut-être cancérogène pour l'homme[13] | |
| Écotoxicologie | |
| LogP | 2,64[1] |
| Seuil de l’odorat | bas : 140 ppm haut : 584 ppm[16] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le tétrachlorométhane ou tétrachlorure de carbone est un composé chimique chloré de formule brute : CCl4. À pression et température ambiante, c'est un liquide incolore, très volatil dont les vapeurs sont nocives pour les êtres vivants. C'est aussi un polluant dangereux pour la couche d'ozone. Il a longtemps été utilisé pour la synthèse de fluides frigorifiques et comme solvant. Son utilisation diminue depuis plusieurs décennies à cause de contraintes environnementales et toxicologiques.
Propriétés
[modifier | modifier le code]CCl4 est une molécule comportant un atome de carbone central, et 4 atomes de chlore reliés au carbone par des liaisons covalentes. L'ensemble forme un tétraèdre parfait. Cette molécule fait donc partie des halométhanes comme CF4. Le tétrachlorométhane est donc apolaire, ce qui le rend apte à solubiliser des molécules telles que des huiles ou des graisses.
Sa pression de vapeur saturante à température ambiante est relativement élevée : 119,4 hPa avec une odeur caractéristique typique des hydrocarbures chlorés. Par rapport à d'autres solvants organiques, CCl4 a une densité élevée, largement supérieure à celle de l'eau : 1,59.
Le tétrachlorométhane a une constante molale ébullioscopique de 5,26 °C1 kg1 mol−1[17].
Synthèse
[modifier | modifier le code]On distingue deux grandes familles de procédés de synthèse: celui qui utilise le méthane comme substrat de départ et celui qui utilise le méthanol[18]. Le premier est basé sur la chloration du méthane par le dichlore:
CH4 + Cl2 → CH3Cl + HCl
Le second utilise l'acide chlorhydrique:
CH3OH + HCl → CH3Cl + H2O
Dans les deux cas, une fois que l'on a obtenu le chlorure de méthyle, on poursuit la synthèse en utilisant le dichlore:
CH3Cl + Cl2 → CH2Cl2 + HCl
CH2Cl2 + Cl2 → CHCl3 + HCl
CHCl3 + Cl2 → CCl4 + HCl
Ce sont des réactions radicalaires qui peuvent être initiées soit de façon thermique en chauffant autour de 400°C, soit en ajoutant un initiateur comme l'AIBN.
Usages
[modifier | modifier le code]En chimie organique, le tétrachlorométhane était souvent employé en tant que solvant. Du fait de sa toxicité (hépatotoxicité et néphrotoxicité), il est souvent remplacé par d'autres solvants moins toxiques comme le chloroforme ou le dichlorométhane.
CCl4 est aussi un fluide utilisable dans les installations de réfrigération, il était connu sous le code R10, Halon 104 ou fréon 10. Il est aujourd'hui interdit pour cet usage du fait de sa forte toxicité et de son action sur la couche d'ozone.
Dangerosité et interdiction
[modifier | modifier le code]En raison de son atteinte à la couche d'ozone, cette substance est interdite au niveau mondial en un usage industriel massif par le protocole de Montréal depuis 1985 mais sa présence dans l’atmosphère a diminué moins vite que prévu et en 2014 une augmentation inexpliquée a même été constatée[19]. En 2011, l'industrie Arkema Mont a rejeté 118 tonnes de tétrachlorure de carbone, soit 7 fois plus que le seuil toléré pour l'ensemble du territoire européen[20].
Les effets de tétrachlorure de carbone sur la santé humaine et l'environnement ont été évalués au titre de REACH en 2012 dans le cadre de l'évaluation de substance par la France. Par la suite, des informations complémentaires ont été demandées aux producteurs, mais plus tard cette décision a été renversée[21].
Un lien significatif entre l’exposition au tétrachlorométhane et le risque de survenue de la maladie de Parkinson est établi[22].
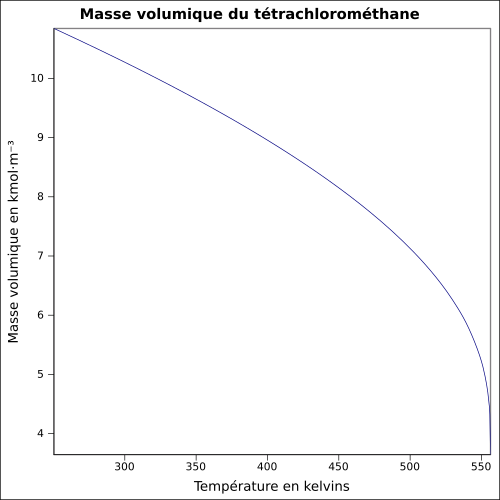
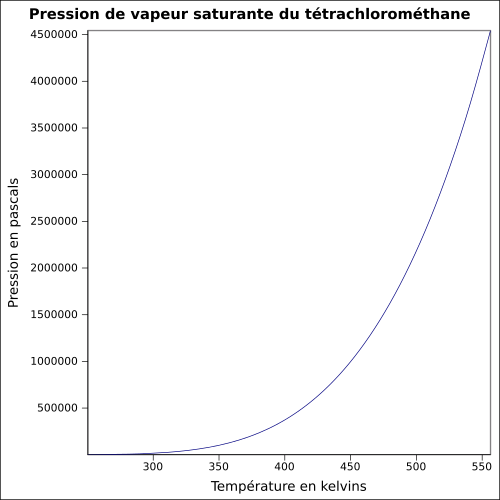
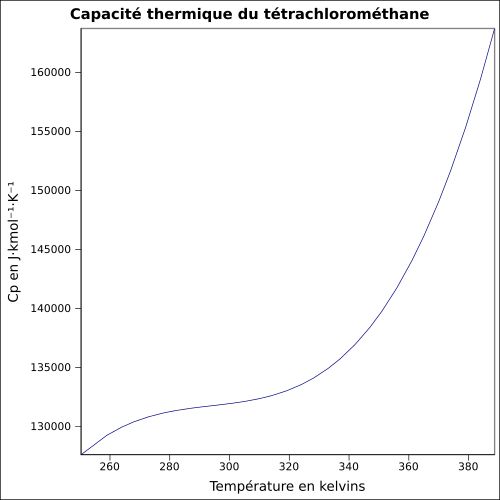
Propriétés physiques
[modifier | modifier le code]Composés apparentés
[modifier | modifier le code]- Chlorométhane
- Dichlorométhane
- Chloroforme (ou trichlorométhane)
- Tétrachlorure de silicium
Notes et références
[modifier | modifier le code]- TETRACHLORURE DE CARBONE, Fiches internationales de sécurité chimique
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, England, John Wiley & Sons Ltd, , 239 p. (ISBN 0-471-98369-1, EAN 978-0-471-98369-9, LCCN 98018212)
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée du numéro CAS « 56-23-5 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 18 novembre 2008 (JavaScript nécessaire)
- (en) James E. Mark, Physical Properties of Polymer Handbook, Springer, , 2e éd., 1076 p. (ISBN 0387690026, lire en ligne), p. 294
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, USA, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5, EAN 978-0-07-049841-9, LCCN 96051648), p. 2-50
- « Properties of Various Gases », sur flexwareinc.com (consulté le )
- (en) W. M Haynes, Handbook of chemistry and physics, Boca Raton, CRC, 2010-2011, 91e éd., 2610 p. (ISBN 978-1-4398-2077-3), p. 14-40
- (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams, vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., (ISBN 0-88415-857-8, 978-0-88415-858-5 et 978-0-88415-859-2)
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- « Carbon tetrachloride », sur reciprocalnet.org (consulté le )
- « tétrachlorure de carbone », sur ESIS, consulté le 23 février 2009
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, « Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme », sur monographs.iarc.fr, CIRC, (consulté le )
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- « Tétrachlorure de carbone » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- « Carbon tetrachloride », sur hazmap.nlm.nih.gov (consulté le )
- P. W. Atkins, Physical Chemistry, 4th Ed., Oxford University Press, (ISBN 0-19-855284-X), C17 (Table 7.2)
- R. Commandeur, « Chlorométhanes », Techniques de l'Ingénieur, , article no J6230 V1
- AFP, « Un polluant interdit depuis 25 ans présent en quantité inexpliquée dans l'atmosphère », Le Monde.fr, (ISSN 1950-6244, lire en ligne)
- « Quand l’État reste impuissant face aux rejets de substances très toxiques par les industriels », sur Basta ! (consulté le )
- « Substance evaluation - CoRAP - ECHA », sur europa.eu (consulté le ).
- (en) Samuel M. Goldman, Patricia J. Quinlan, G. Webster Ross et Connie Marras, « Solvent exposures and parkinson disease risk in twins », Annals of Neurology, vol. 71, no 6, , p. 776–784 (ISSN 0364-5134, PMID 22083847, PMCID PMC3366287, DOI 10.1002/ana.22629, lire en ligne, consulté le )
Voir aussi
[modifier | modifier le code]Articles connexes
[modifier | modifier le code]- Margo Jones (1911-1955), pionnière du théâtre au Texas, victime du tétrachlorométhane.