Talium(III) oksida
| |
| Nama | |
|---|---|
| Nama lain
talium trioksida, talium sesquioksida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat[1] | |
| Tl2O3 | |
| Massa molar | 456.76 g/mol |
| Penampilan | padatan cokelat gelap |
| Densitas | 10.19 g/cm3, padat (22 °C) |
| Titik lebur | 717 °C (1.323 °F; 990 K) |
| Titik didih | 875 °C (1.607 °F; 1.148 K) (terurai) |
| tidak larut | |
| +76.0·10−6 cm3/mol | |
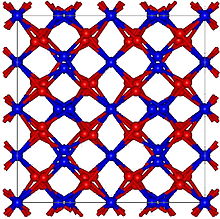
| Struktur | |
| Kubik, (Bixbyite) cI80[2] | |
| Ia3 (No. 206) | |
| Bahaya | |
| Piktogram GHS |   
|
| Keterangan bahaya GHS | {{{value}}} |
| <abbr class="abbr" title="Error in hazard statements">HH300 + H330, <abbr class="abbr" title="Error in hazard statements">HH373, <abbr class="abbr" title="Error in hazard statements">HH411 | |
| <abbr class="abbr" title="Error in hazard statements">PP273, <abbr class="abbr" title="Error in hazard statements">PP301 + P310 + P330, <abbr class="abbr" title="Error in hazard statements">PP304 + P340 + P310, <abbr class="abbr" title="Error in hazard statements">PP314 | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
44 mg/kg (oral, rat) |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Talium(III) oksida adalah senyawa kimia talium dan oksigen. Itu tersedia di alam sebagai mineral langka avisenit.[4] Strukturnya terkait dengan Mn2O3 yang memiliki struktur seperti bixbyite. Tl2O3 adalah logam dengan konduktivitas tinggi dan merupakan semikonduktor tipe-n degenerasi yang berpotensi digunakan dalam sel surya.[5] Sebuah metode produksi Tl2O3 oleh MOCVD diketahui.[6] Setiap penggunaan praktis talium(III) oksida harus selalu memperhitungkan sifat beracun talium. Kontak dengan uap air dan asam dapat membentuk senyawa talium yang beracun.
Produksi
Talium(III) oksida dihasilkan oleh reaksi talium dengan oksigen atau hidrogen peroksida dalam larutan alkali talium(I). Atau, dapat dibuat dengan oksidasi talium(I) nitrat oleh klorin dalam larutan kalium hidroksida encer.[7]
Referensi
- ^ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (edisi ke-62nd). Boca Raton, FL: CRC Press. hlm. B156. ISBN 0-8493-0462-8..
- ^ Otto H.H.; Baltrasch R.; Brandt H.J. (1993). "Further evidence for Tl3+ in Tl-based superconductors from improved bond strength parameters involving new structural data of cubic Tl2O3". Physica C. 215 (1–2): 205. doi:10.1016/0921-4534(93)90382-Z.
- ^ GHS: Sigma-Aldrich 204617
- ^ http://www.handbookofmineralogy.org/pdfs/avicennite.pdf Handbook of Mineralogy
- ^ Phillips R. J.; Shane M. J.; Switzer J. A. (1989). "Electrochemical and photoelectrochemical deposition of Thallium(III) Oxide thin films". Journal of Materials Research. 4 (4): 923. doi:10.1557/JMR.1989.0923.
- ^ D. Berry; R. T. Holm; R. L. Mowery; N. H. Turner; M. Fatemi (1991). "Thallium(III) Oxide by Organometallic Chemical Vapor Deposition". Chemistry of Materials. 3 (1): 72–77. doi:10.1021/cm00013a019.
- ^ Georg Brauer; Handbuch der präparativen anorganischen Chemie, Band 2, S.884; ISBN 3-432-87813-3 (in German)
