سيلان (مركب كيميائي)
المظهر
| سيلان (مركب كيميائي) | |
|---|---|
 |
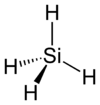 |
| الاسم النظامي (IUPAC) | |
Silane |
|
| أسماء أخرى | |
Monosilane, Silicane, Silicon hydride, Silicon tetrahydride |
|
| المعرفات | |
| CAS | 7803-62-5[1] |
| بوب كيم | 23953[2] |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | SiH4 |
| الكتلة المولية | 32.12 غ/مول |
| المظهر | غاز عديم اللون |
| الكثافة | 1.44 غ/سم3 |
| نقطة الانصهار | −185 °س |
| نقطة الغليان | −112 °س |
| الذوبانية في الماء | يتفاعل |
| المخاطر | |
| رمز الخطر وفق GHS |   |
| وصف الخطر وفق GHS | خطر |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
السيلان هو مركب غير عضوي صيغتة الكيميائية SiH4 ويوجد على شكل غاز عديم اللون. يعد المركب أبسط مركبات السيلانات، وهو مشابه بنيوي للميثان.
التحضير
[عدل]يمكن أن يحضر المركب بعدة طرق،[4] منها تفاعل رباعي كلوريد السيليكون مع هيدريد الليثيوم:
أو بتفاعل سيليسيد المغنيسيوم مع حمض الهيدروكلوريك.
الخواص
[عدل]يوجد المركب في الشروط القياسية على شكل غاز عديم اللون، وهو حساس تجاه الأكسجين حيث يحترق تلقائياً بشكل ناشر للحرارة:
ويتفاعل مع الماء والرطوبة:
ويتفكك بالتسخين فوق الدرجة 300 °س بمعزل عن الهواء والرطوبة إلى مكوناته الأولية:
الاستخدامات
[عدل]يستخدم المركب من أجل الحصول على السيليكون مرتفع النقاوة، حيث أنتج منه حوالي 300 طن سنوياً أواخر تسعينيات القرن العشرين.[5] تجرى محاولات لإعادة تدويره في مثل تلك التطبيقات.[6][7]
طالع أيضاً
[عدل]مراجع
[عدل]- ^ silane، معهد المعلوماتية الحيوية الأوروبي، QID:Q902623
- ^ ا ب ج د Silicon hydride (بالإنجليزية), QID:Q278487
- ^ ChEBI release 2020-09-01، 1 سبتمبر 2020، QID:Q98915402
- ^ Simmler, W. (2005)، "Silicon Compounds, Inorganic"، موسوعة أولمان للكيمياء الصناعية، فاينهايم: وايلي-في سي إتش، DOI:10.1002/14356007.a24_001
- ^ Timms, P. L. (1999). "The chemistry of volatile waste from silicon wafer processing". Journal of the Chemical Society, Dalton Transactions ع. 6: 815–822. DOI:10.1039/a806743k.
- ^ Briend P, Alban B, Chevrel H, Jahan D. American Air, Liquide Inc. (2009) "Method for Recycling Silane (SiH4)". US20110011129 نسخة محفوظة 2013-09-22 على موقع واي باك مشين., EP2252550A2 نسخة محفوظة 2013-09-23 على موقع واي باك مشين..
- ^ Kreiger، M.A.؛ Shonnard، D.R.؛ Pearce، J.M. (2013). "Life cycle analysis of silane recycling in amorphous silicon-based solar photovoltaic manufacturing". Resources, Conservation and Recycling. ج. 70: 44–49. DOI:10.1016/j.resconrec.2012.10.002. مؤرشف من الأصل في 2017-11-12.
في كومنز صور وملفات عن Silane.






