Adenozin-monofosfat
| Adenozin-monofosfat | |||
|---|---|---|---|
| |||
| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 61-19-8 | ||
| ChemSpider[1] | 5858 | ||
| UNII | 415SHH325A | ||
| MeSH | |||
| IUPHAR ligand | 2455 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C10H14N5O7P | ||
| Molarna masa | 347,22 g/mol | ||
| pKa | 0.9, 3.8, 6.1 | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
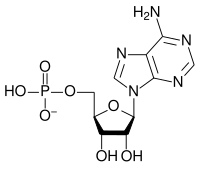
Adenozin monofosfat (AMP), ili 5'-adenilna kiselina, je nukleotid koji je RNK gradivni blok. Ovo jedinjenje je ester fosforne kiseline i nukleozida adenozina. AMP se sastoji od fosfatne grupe, šećera riboze, i nukleobaze adenina.[2][3] Kao supstituent on se označava prefiksom adenilil-.
AMP se može proizvesti tokom ATP sinteze enzimom adenilat kinaza kombinovanjem dva ADP molekula[4]:
- 2 ADP → ATP + AMP
Alternativno AMP se može proizvesti hidrolizom jedne visokoenergijske fosfatne ADP veze:
- ADP → AMP + Pi
AMP može takođe biti formiran hidrolizom ATP u AMP i pirofosfat[5]:
- ATP → AMP + PPi
Kad se RNK razlaže u živim sistemima, nukleozid monofosfati, poput adenozin monofosfata, se formiraju.
AMP se može regenerisati u ATP na sledeći način:
- AMP + ATP → 2 ADP (adenilat kinaza u suprotnom pravcu)
- ADP + Pi → ATP (ovaj step se najčešće izvodi u aerobima putem ATP sintaze tokom oksidativne fosforilacije)
AMP može biti konvertovan u IMP enzimom mioadenilat deaminaza, odstranjenjem jedne amino grupe.
U kataboličkim putevima, adenozin monofosfat može biti konvertovan u uričnu kiselinu, koja se izlučuje iz tela.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Даринка Кораћевић, Гордана Бјелаковић, Видосава Ђорђевић. Биохемија. савремена администрација. ISBN 86-387-0622-7.
- ↑ David L. Nelson, Michael M. Cox (2005). Principles of Biochemistry (4th izd.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ↑ Rosano TG, Clayson KJ, Strandjord PE (July 1976). „Evaluation of adenosine 5'-monophosphate and fluoride as adenylate kinase inhibitors in the creatine kinase assay”. Clin. Chem. 22 (7): 1078–83. PMID 179733.
- ↑ Kunitz M (March 1962). „Hydrolysis of adenosine triphosphate by crystalline yeast pyrophosphatase. Effect of zinc and magnesium ions”. J. Gen. Physiol. 45(4)Pt 2: 31–46. PMC 2195188. PMID 14460583.
- Ming D, Ninomiya Y, Margolskee RF (August 1999). „Blocking taste receptor activation of gustducin inhibits gustatory responses to bitter compounds”. Proc. Natl. Acad. Sci. U.S.A. 96 (17): 9903–8. PMC 22308. PMID 10449792.
- Даринка Кораћевић, Гордана Бјелаковић, Видосава Ђорђевић. Биохемија. савремена администрација. ISBN 86-387-0622-7.
