Rikkihappo
| Rikkihappo | |
|---|---|
 |
|
 |
|
| Tunnisteet | |
| Muut nimet | Vihtrilliöljy |
| CAS-numero | |
| PubChem CID | |
| Ominaisuudet | |
| Molekyylikaava | H2SO4 |
| Moolimassa | 98,08 g/mol |
| Ulkomuoto | Kirkas, väritön tai ruskea ja hajuton neste |
| Sulamispiste | 10 °C (283 K) |
| Kiehumispiste | 337 °C (610 K) |
| Tiheys | 1,8 g/cm3 |
| Liukoisuus veteen | Liukenee kokonaan |

Rikkihappo (H2SO4, vihtrilliöljy) on vahva, veteen täysin liukeneva epäorgaaninen happo. Se on puhtaana kirkas, huoneenlämmössä hieman jähmeäjuoksuinen neste, jonka tiheys on 1,83-kertainen veden tiheyteen verrattuna. Rikkihappo on voimakkaasti syövyttävää.[1]
Rikkihappo on yksi ensimmäisistä teollisesti valmistetuista kemikaaleista. Sitä on valmistettu teollisesti jo 1700-luvulta lähtien. Nykyään rikkihappo on yksi maailman tärkeimmistä ja käytetyimmistä kemiallisista yhdisteistä. Vuonna 2005 rikkihappoa kulutettiin maailmanlaajuisesti 190 miljoonaa tonnia. Noin puolet rikkihaposta käytetään lannoitteiden valmistamiseen ja loppu hyödynnetään väriaineiden, lääkkeiden ja räjähteiden valmistuksessa sekä öljynjalostuksessa ja metallurgisissa prosesseissa.[2] Rikkihappoa käytetään myös lyijyakkujen elektrolyyttinä. Koska rikkihappo on merkittävä teollisuudessa, sen maakohtaista kulutusta on pidetty yhtenä talouden mittarina. Rikkihapon kulutus on vaihdellut runsaasti, mutta koko maailmassa sen kulutus lisääntyy jatkuvasti.[3]
Historia
[muokkaa | muokkaa wikitekstiä]
Rikkihappoa kutsutaan joskus myös vihtrilliöljyksi. Nimi periytyy aineista, joita käytettiin ennen nykyaikaisia menetelmiä rikkihapon valmistuksessa. Ennen rikkihappoa valmistettiin polttamalla joko rauta(II)sulfaattiheptahydraattia (FeSO4·7H2O) eli vihreää vihtrilliä tai kupari(II)sulfaattipentahydraattia (CuSO4·5H2O) eli sinistä vihtrilliä. Poltossa syntyi vettä ja rikkitrioksidia, jotka reagoidessaan muodostivat öljymäistä ainetta eli rikkihappoa.[4]
Rikkihapon löytäjästä ei ole yksimielisyyttä. Rikkihapon varhaisin löytäjä saattaa olla persialainen lääkäri Mohammad al-Razi, joka tunnetaan myös etanolin löytäjänä ja joka osasi hyödyntää sitä puhdistusaineena. Rikkihapon hän löysi kuivatislatessaan rikkiä sisältänyttä mineraalia. Yleisnerona tunnettu persialainen Geber nimetään myös monesti rikkihapon löytäjäksi. Hänen kerrotaan löytäneen suolahapon sekoittamalla rikkihappoa ja ruokasuolaa. Eurooppalaiset keksivät aineen vasta 1500-luvulla Jan Baptist van Helmontin tekemien kokeiden ansiosta. On tosin väitetty Vincent Beauvais'laisen ja Albert Suuren tunteneen yhdisteen.[5]
Rikkihappo liittyy keskeisesti vedyn löytöhistoriaan. Robert Boyle pani 1600-luvun puolivälin paikkeilla rautanauloja rikkihappoon ja havaitsi, että reaktiossa vapautuu runsaasti kaasumaista vetyä. Alkuaineeksi vedyn totesi Henry Cavendish pudoteltuaan rauta-, tina- ja sinkkipalasia suolahappoon ja rikkihappoon.[6]

Rikkihapon tärkeys ymmärrettiin nopeasti, ja se oli yksi ensimmäisistä kemikaaleista, joita tuotettiin suuremmassa määrin. Tässä ansioitui erityisesti lontoolaisapteekkari Joshua Ward, joka käytti saksalais-hollantilaisen Johann Glauberin tekniikkaa. Glauber valmisti rikkihappoa polttamalla rikkiä ja kaliumnitraattia vesihöyryä sisältävässä astiassa. Glauber keksi myös keinon, jolla rikkihapon avulla voidaan valmistaa typpihappoa. Tekniikkaa paranteli vuonna 1746 lääkäri John Roebuck suorittamalla reaktiot lyijykammiossa, jotka olivat kestävämpiä, suurempia ja edullisempia kuin aiemmat lasiastiat. Alan uranuurtajiin kuului myös Johann Christian Bernhardt. Yhdysvalloissa rikkihappo oli ensimmäisiä kemikaaleja, joita alettiin tuottaa kaupallisesti.[5]
Lyijykammiomenetelmällä oli kuitenkin omat heikkoutensa. Louis-Joseph Gay-Lussac ja John Glover tekivät prosessiin parannuksia, joiden ansiosta rikkihaposta saatiin 78-prosenttista, mutta se ei edelleenkään ollut tarpeeksi väkevää kaikkiin tarkoituksiin. Vasta 1800-luvun alussa Peregrine Phillips keksi kontaktimenetelmän, jolla syntyi väkevämpää happoa. Kontaktimenetelmä yleistyi hitaasti, mutta se on erilaisine muunnelmineen nykyisen rikkihappotuotannon perusta.[7]
Rikkihaposta on tullut niin olennainen osa teollistunutta yhteiskuntaa, että sen kulutusta pidetään teollistuneisuuden mittana. Voimakkaasti teollistuneessa valtiossa rikkihapon kulutus on suurempaa kuin vähemmän teollistuneessa.[8]
Ominaisuudet
[muokkaa | muokkaa wikitekstiä]Turvaohjeet
[muokkaa | muokkaa wikitekstiä]
Rikkihappo on huoneenlämmössä voimakkaasti syövyttävää, kirkasta, hajutonta ja öljymäistä nestettä. Se reagoi voimakkaasti useimpien metallien kanssa synnyttäen helposti syttyvää vetykaasua. Huoneenlämmössä se haihtuu hitaasti, eikä siitä vapaudu ärsyttäviä höyryjä. Vaikka rikkihappo ei ole syttyvää, se voi saada aikaan tulipalon sytyttämällä ympärillä olevaa ainetta.[9]
Kuuma rikkihappo on vaaraksi läsnäolijoiden silmille ja hengitysteille. Kuumasta rikkihaposta vapautuu rikkidioksidia ja syövyttäviä rikkihappohöyryjä. Lisäksi esimerkiksi lyijyakun lataaminen muodostaa hengitysteitä polttavaa rikkihapposumua. Rikkihapporoiskeet on huuhdeltava välittömästi silmistä ja iholta runsaalla vedellä. Väkevä happoliuos voi aiheuttaa vakavan silmävaurion ja syövyttää ihoa aiheuttaen tuskallisia haavoja. Kun ensiapu on annettu, rikkihapolle altistuneen tulee hakeutua lääkärin hoitoon.[9][10]
Kun rikkihappoa liukenee veteen, vapautuu runsaasti lämpöenergiaa. Tämän vuoksi rikkihappo, kuten kaikki muutkin hapot, laimennetaan aina siten, että happoa kaadetaan veteen. Koskaan ei saa kaataa vettä rikkihappoon, sillä silloin vesi voisi alkaa kiehua hapon pinnalla ja aiheuttaa roiskumista. Tästä juontuukin sanonta: "Ensin vesi, sitten happo, muuten tulee käteen rakko."[11] Rikkihapon aiheuttamaa tai happoliuoksen lähellä olevaa tulipaloa sammutettaessa on siis varottava veden joutumista happoon.
Jätteeksi jäänyt rikkihappo laimennetaan varovasti vedellä ja neutraloidaan kalkilla.[9]
Fysikaaliset ominaisuudet
[muokkaa | muokkaa wikitekstiä]Rikkihapon väri vaihtelee kellertävästä ja ruskeasta täysin kirkkaaseen riippuen sen puhtausasteesta. Normaalissa ilmanpaineessa ja huoneenlämmössä rikkihappo on nestemäistä ainetta, jonka suuri viskositeetti aiheuttaa sen öljymäisen luonteen. Rikkihapon viskositeetti on 27 500·10−6 Ns/m², kun vedellä se on 1040·10−6 Ns/m².[12] Normaalissa ilmanpaineessa puhtaan rikkihapon sulamispiste on 10,36 °C ja tiheys 1,832 g/cm³.[13] Puhdasta rikkihappoa ei kuitenkaan ole kaupallisesti saatavilla, vaan sitä myydään eri konsentraatioissa, joiden termodynaamiset ominaisuudet ovat selvästi erilaisia puhtaaseen aineeseen verrattuna. Väkevimmän eli 98-prosenttisen rikkihapon sulamispiste on 3 °C, kiehumispiste 338 °C ja tiheys hieman suurempi, 1,84 g/cm³. Puhdas rikkihappo hajoaa lämmitettäessä rikkitrioksidiksi ja vedeksi, kunnes se saavuttaa 98,3 prosentin väkevyyden. Tämän liuoksen kiehumispiste on noin 337–338 °C. Lämmitettäessä edelleen rikkihappo hajoaa kokonaan edellä mainituiksi lopputuotteiksi.[14][15]
Kemialliset ominaisuudet
[muokkaa | muokkaa wikitekstiä]
Rikkihappo on kaksiarvoinen happo, koska sen molekyylissä on kaksi vetyatomia, jotka voivat irrota protolyysireaktiossa. Protolyysireaktio tapahtuu kahdessa osassa. Rikkihapolla on siksi kahdentyyppisiä suoloja. Rikkihapon suolat ovat nimeltään sulfaatteja tai vetysulfaatteja (SO42− on sulfaatti-ioni, HSO4−, vetysulfaatti-ioni). Konsentraatioltaan yksimolaarisessa vesiliuoksessa rikkihappo luovuttaa toisen protoneistaan eli protolysoituu käytännöllisesti katsottuna täydellisesti vetysulfaatti-ioneiksi seuraavan reaktioyhtälön mukaisesti:
- H2SO4 + H2O → HSO4− + H3O+
Vetysulfaatti-ioni on huomattavasti heikompi happo kuin rikkihappo, eivätkä kaikki vetysulfaatti-ionit siis luovuta protonia:
- HSO4− + H2O → SO42− + H3O+
Vain noin 1,3 % vetysulfaatti-ioneista on protolysoitunut sulfaatti-ioneiksi yksimolaarisessa rikkihappoliuoksessa.[16]
Vetyionit (eli positiiviset yhden protonin vety-ytimet) eivät viihdy yksin vedessä vaan liittyvät heti vesimolekyyleihin. Tällöin muodostuu positiivisia oksoniumioneja, H3O+. Oksoniumionien suuri konsentraatio liuoksessa aiheuttaa happamuuden.[17]
Epäjalot metallit, jotka sijaitsevat metallien sähkökemiallisessa jännitesarjassa ennen vetyä, reagoivat jo laimean rikkihapon kanssa. Tällöin hapon vetyatomit pelkistyvät, ja reaktiossa syntyvän metallisulfaatin lisäksi muodostuu myös vetykaasua. Epäjalot metallit, jotka muodostavat ionin hapetusluvulla +II, reagoivat rikkihapon kanssa seuraavasti (M merkitsee tässä mielivaltaista metallia):
- M(s) + H2SO4(aq) → MSO4(aq) + H2(g)[18]
Jalot metallit sijaitsevat jännitesarjassa vedyn jäljessä, joten vetyionit eivät kykene hapettamaan niitä, eivätkä ne liukene laimeaan rikkihappoliuokseen vetyä vapauttaen. Sen sijaan jaloista metalleista kupari, elohopea ja hopea liukenevat väkevään rikkihappoon, joka on erittäin vahva hapetin. Tällöin pelkistyy vetyatomien sijasta osa rikkihapon rikkiatomeista rikkidioksidiksi.
- Cu(s) + 2 H2SO4(aq) → CuSO4(aq) + SO2(g) + 2 H2O(l)
Erittäin jalot metallit kuten platina ja kulta eivät reagoi hapettuen edes väkevän rikkihapon kanssa.[18] Vaikka lyijy on epäjalo metalli, laimea rikkihappo ei kykene juurikaan liuottamaan sitä. Tämä johtuu siitä, että lyijyn ja rikkihapon reaktiossa syntyvä lyijysulfaatti on erittäin niukkaliukoista ja muodostaa lyijymetallin päälle suojaavan kerroksen. Erittäin väkevä ja noin 260-asteinen kuuma rikkihappo sen sijaan liuottaa myös lyijymetallin täydellisesti.[19]

Väkevä rikkihappo sitoo hyvin vettä. Tästä syystä rikkihappoa voidaan käyttää myös kuivausaineena esimerkiksi kaasujen valmistuksessa. Muun muassa valmistettaessa kloorikaasua alkalimenetelmällä on tuotteessa mukana usein vesihöyryä. Höyry poistetaan johtamalla kaasuseos väkevään rikkihappoon.[20] Vastaavalla tavalla, johtamalla väkevään typpihappoon, voidaan kuivata useita muitakin kaasuja, kuten happea, typpeä ja hiilidioksidia.[21]
Rikkihappo voi imeä itseensä vettä myös kiinteistä orgaanisista yhdisteistä hajottamalla niitä. Esimerkiksi hiilihydraatit koostuvat hiilestä, hapesta ja vedystä. Paperi koostuu pääasiassa selluloosasta, joka on hiilihydraatti. Kun paperin päälle kaadetaan väkevää rikkihappoa, paperi mustuu. Rikkihappo hajottaa paperin selluloosaa ja ryöstää siltä veden alkuaineet, vedyn ja hapen. Jäljelle jää hiili, joka antaa paperille mustan värin.[22]
Piidioksidin ja silikaattien kanssa rikkihappo ei reagoi, minkä vuoksi sitä voidaankin säilyttää lasiastioissa.
Valmistus
[muokkaa | muokkaa wikitekstiä]Tuotanto ja hinta
[muokkaa | muokkaa wikitekstiä]
Rikkihapon maailmanlaajuinen tuotanto kasvaa koko ajan. 2000-luvun alussa se oli 170 miljoonaa tonnia vuodessa.[4] Suurimman tuottajamaan Yhdysvaltojen vuosittainen rikkihappotuotanto on pysynyt jo pidempään 40 miljoonassa tonnissa.[24] Vaikka tuotantokapasiteetti kasvaa koko ajan, rikkihapon hinta kohosi vuonna 2007 ennätyslukemiin, melkein 90:een Yhdysvaltain dollariin per nettotonni.[25] Seuraavana vuonna hinta melkein nelinkertaistui, mutta laski vuoden loppuun mennessä noin 200 dollariin per tonni.[26][27] Uusien tuotantolaitosten kapasiteetti on mittava. Saudi-Arabiaan on suunniteltu rakennettavan maailman suurin tuotantolaitos, joka pystyy tuottamaan jopa 13 500 tonnia rikkihappoa päivässä eli täydellä kapasiteetillaan toimiessaan noin 49 miljoonaa tonnia vuodessa. Suomalaisen Outotecin toimittaman laitoksen arvellaan valmistuvan vuonna 2010.[28]
Rikkihapon kulutus kasvoi 25 % vuosien 1990 ja 2008 välillä. Vuonna 2008 suurimpia rikkihapon kuluttajia olivat Aasian maat, jotka kuluttivat noin 28 % vuonna 2008 tuotetusta rikkihaposta. Yhdysvallat on toiseksi suurin rikkihapon käyttäjä 19 % osuudella ja Afrikan maat kuluttavat noin 10 % kaikesta tuotetusta haposta. Länsi-Euroopan ja Keski- sekä Etelä-Amerikan valtiot kuluttavat rikkihappoa suunnilleen saman verran, molemmat 6–8 % kaikesta rikkihappotuotannosta.[3]
Rikkihapon kulutuksen kasvua on hyvin vaikea arvioida, ja se riippuu suuresti lannoitemarkkinoista. On arvioitu, että rikkihapon tuotanto tulee kasvamaan 1,4 % vuosittain vuosien 2008 ja 2015 välillä.[3]
Valmistusmenetelmät
[muokkaa | muokkaa wikitekstiä]
Teollisuudessa rikkihappoa valmistetaan nykyisin hapettamalla rikkidioksidia rikkitrioksidiksi ja antamalla sen reagoida veden kanssa. Rikkidioksidia saadaan polttamalla rikkiä, pasuttamalla eli kuumentamalla ilmavirrassa sulfidimineraaleja kuten rikkikiisua eli rautasulfidia tai hapettamalla divetysulfidia.[24]
- S(s) + O2(g) → SO2(g)
- 4 FeS(s) + 7 O2(g) → SO2(g) + 2 Fe2O3(s)
- 2 H2S(g) + 3 O2(g) → 2 SO2(g) + 2 H2O

Rikkidioksidi hapetetaan rikkitrioksidiksi. Apuna käytetään katalyyttiä, koska muuten hapettuminen olisi hyvin hidasta. Peregrine Phillips keksi ensimmäisenä katalyytin (platina) hyödyn vuonna 1830, mutta hänen kehittämänsä kontaktimenetelmä levisi hitaasti laajempaan käyttöön, ja heikkosaantoisempi John Roebuckin reaktiomekanismiltaan eroava lyijykammioprosessi säilyi käytetyimpänä prosessina pitkään. Nykyiset teollisuusprosessit ovat Phillipsin kontaktiprosessin erilaisia muunnelmia. Aikaisemmin rikkihapon valmistuksessa katalyyttinä käytettiin lyijykammiomenetelmässä typpidioksidia, mutta nykyisin kontaktimenetelmässä käytetyin katalyytti on divanadiinipentoksidi. Kontaktiprosessissa rikkitrioksidikaasu johdetaan erittäin väkevään 98-prosenttiseen rikkihappoliuokseen.[24]
- 2 SO2(g) + O2(g) → 2 SO3(g)
- SO3(g) + H2O(l) → H2SO4(aq)
Lyijykammiomenetelmä
[muokkaa | muokkaa wikitekstiä]
- Pääartikkeli: Lyijykammiomenetelmä
1800-luvun alkupuolelle asti rikkihappoa tuotettiin lasipulloihin.[29] John Roebuckin kehittämän lyijykammiomenetelmän myötä rikkihapon teollinen tuotanto käynnistyi laajemmassa mittakaavassa. Prosessissa rikkidioksidi kerättiin suuriin kammioihin, joiden seinät oli vuorattu lyijylevyillä. Lyijy on yksi harvoista rikkihappoa kestävistä metalleista.[30] Alkuperäisessä lyijykammioprosessissa kuumennettiin kaliumnitraattia rikin kanssa, jolloin vapautui rikin oksideja ja typpimonoksidia. Tämän jälkeen kammioon päästettiin vettä, joka reagoi rikkitrioksidin kanssa muodostaen rikkihappoa.[29] Menetelmää parantelivat muun muassa Charles Bernard Desormes ja Nicolas Clément sekä Charles Tennant, joka keksi erillisen rikinpolttokammion. John Gloverin ja Joseph-Louis Gay-Lussacin tekniset parannukset mahdollistivat aiempaa selvästi väkevämmän hapon tuotannon. Vuonna 1818 Hill of Deptford käytti rikin lähteenä pyriittimalmeja. Tavasta tuli yleinen kaksikymmentä vuotta myöhemmin.[30]
Rikkihapon valmistus lyijykammiomenetelmässä perustuu rikkidioksidin hapettumiseen katalyyttinä toimivan typpimonoksidin avulla. Kemialliset reaktiot lyijykammiomenetelmässä ovat kuitenkin monimutkaisia, eikä kaikista reaktiomekanismeista ole yksimielisyyttä. Yleisesti välituotteena katsotaan syntyvän nitrosyylirikkihappoa.[31]
Lyijykammiomenetelmällä tuotettava rikkihappo on väkevyydeltään 62–77-prosenttista. Siinä on usein epäpuhtauksina typpihappoa, typpihapoketta, lyijysulfaattia, seleenihapoketta, arseenitrioksidia sekä pieniä määriä metalleja.[31]
Kontaktimenetelmä
[muokkaa | muokkaa wikitekstiä]- Pääartikkeli: Kontaktimenetelmä
Viinietikkakauppias Peregrine Phillipsin vuonna 1831 patentoimassa kontaktimenetelmässä rikkidioksidi hapetetaan rikkitrioksidiksi katalyytin avulla. Prosessin nimi tulee siitä, että rikkidioksidi ja happi saadaan ”kontaktiin” katalyytin avulla. Nykyisin useimmiten käytettävä katalyytti on divanadiinipentoksidi. Rikkidioksidi johdetaan reaktiokammioon, jonka lämpötila on 400–450 °C ja paine on yhdestä kahteen ilmakehän painetta. Näissä oloissa rikkidioksidin katalyyttinen hapettuminen on hyvin tehokasta, noin 99,5 prosenttia rikkidioksidista hapettuu.[32]
Kaavio kontaktimenetelmän vaiheista:
Katalyytti on divanadiinipentoksidin ja kaliumsulfaatin tai -pyrosulfaatin seos piidioksidialustalla. Vanadiinikatalyytti pelkistyy divanadiinitetroksidiksi hapettaen rikkidioksidin rikkitrioksidiksi. Divanadiinitetroksidi reagoi reaktorissa olevan hapen kanssa palautuen divanadiinipentoksidiksi ja uudelleen käytettäväksi.[33]
- SO2 + V2O5 → SO3 + V2O4
- V2O4 + ½ O2 → V2O5
Muodostunut rikkitrioksidi johdetaan väkevään rikkihappoliuokseen, jolloin muodostuu niin sanottua savuavaa rikkihappoa eli pyrorikkihappoa, joka hydrolysoituu rikkihapoksi.[32]
WSA-menetelmä
[muokkaa | muokkaa wikitekstiä]
- Pääartikkeli: WSA-menetelmä
WSA-menetelmä eli märkä rikkihappoprosessi (engl. wet sulfuric acid process) on kontaktimenetelmän johdos, joka kehiteltiin 1960-luvulla. WSA-prosessilla rikkihappoa voidaan valmistaa lähes mistä tahansa kaasumaisesta rikin yhdisteestä. Erityisen hyvin prosessiin soveltuu monissa teollisuusprosesseissa jätteenä syntyvä rikkivety. Rikkipitoinen kaasu poltetaan rikin oksideiksi. Kaasu johdetaan kammioon, jossa rikkidioksidi hapetetaan rikkitrioksidiksi divanadiinipentoksidikatalyytin avulla. Toisin kuin kontaktimenetelmässä WSA-menetelmässä on mukana vesihöyryä, joka reagoi rikkitrioksidin kanssa muodostaen kaasumaista rikkihappoa. Kaasut jäähdytetään ja siirretään kondensaatiotilaan, jossa rikkihappohöyryyn suihkutetaan vettä. Syntynyt rikkihappoliuos jäähdytetään ja kerätään.[34]
Käyttö
[muokkaa | muokkaa wikitekstiä]Yleistä
[muokkaa | muokkaa wikitekstiä]Rikkihappo on eniten käytetty teollisuuskemikaali.[35] Sitä käytetään sellu- ja paperiteollisuudessa, kaivos- ja metalliteollisuudessa sekä kemianteollisuudessa muun muassa fosfaattien, lannoitteiden, titaanidioksidin ja viskoosin valmistukseen.[36] Öljyteollisuudessa rikkihappoa käytetään epäpuhtauksien poistamiseen. Sitä käytetään myös metallipintojen puhdistukseen, malmien käsittelyyn, kemiallisten reaktioiden katalyyttinä ja muiden epäorgaanisten happojen lähtöaineena. Rikkihappoa käytetään myös veden poistamiseen orgaanisista yhdisteistä. Lisäksi sitä voidaan käyttää elintarvikkeissa happamuuden säätöaineena. Sen E-koodi on E513.[37] Suurin osa valmistetusta rikkihaposta käytetään fosfaattilannoitteiden valmistamiseen.[38] Elektroniikkateollisuudelle tärkeiden piikiekkojen puhdistukseen orgaanisista epäpuhtauksista käytetään niin kutsuttua SPM- eli piranha-liuosta, joka sisältää rikkihappoa.[39]
Rikkihapon 25-prosenttista liuosta käytetään lyhttps://www.ruokavirasto.fi/elintarvikkeet/ohjeita-kuluttajille/e-kooditlisaaineet/e-koodit/e513ijyakkujen akkuhappona.[40]
Käyttö lannoitteiden valmistuksessa
[muokkaa | muokkaa wikitekstiä]
Suurin osa lannoitteiden valmistuksessa käytettävästä rikkihaposta kuluu fosfaattien muuttamiseen sen avulla veteen paremmin liukenevaan muotoon.[41] Perinteisessä kalsiumdivetyfosfaatin (Ca(H2PO4)2) eli superfosfaatin valmistuksessa käytetyssä märkäprosessissa kalsiumfosfaattipitoista kiveä käsitellään 93-prosenttisella rikkihappoliuoksella kahdeksan tunnin ajan. Tällöin reaktiotuotteina syntyy kalsiumdivetyfosfaattia ja sivutuotteena kalsiumsulfaattia (CaSO4).[38]
- Ca3(PO4)2 + 2 H2SO4 → Ca(H2PO4)2 + 2 CaSO4
Rikkihappoa käytetään myös toisen tärkeän lannoitteen, ammoniumsulfaatin (NH4)2SO4, valmistukseen. Ammoniumsulfaatin valmistuksessa ammoniakkikaasua (NH3) johdetaan reaktoriin, jossa on kylläistä ammoniakkisulfaattiliuosta ja hieman rikkihappoa. Reaktorin lämpötila on 60 °C. Reaktoriin johdetaan samanaikaisesti väkevää rikkihappoa ylläpitämään vapaan rikkihapon pitoisuus oikeana. Ammoniumsulfaatti kiteytyy kylläisestä liuoksesta reaktorin pohjalle ja voidaan erottaa. Kuivaa ammoniumsulfaattijauhetta voidaan myös valmistaa suihkuttamalla rikkihappoa ammoniakkia sisältävään kammioon.[42]
- 2 NH3 + H2SO4 → (NH4)2SO4
Saksalainen kemisti Justus von Liebig loi tutkimuksillaan pohjan lannoitteiden teolliselle valmistukselle. Rikkihapon käyttöä lannoitteiden valmistuksessa tutki ensimmäisenä James Murray, joka liuotti luita rikkihappoon 1800-luvun alussa. Hänen poikansa John Fischer Murray haki vuonna 1842 patentin menetelmälleen valmistaa lannoitteita kalsiumfosfaatista ja rikkihaposta. John Bennet Lawes patentoi samana vuonna samankaltaisen menetelmän superfosfaattilannoitteiden eli kalsiumdivetyfosfaattilannoitteiden valmistukseen. Lawes oli Murrayta parempi keksintönsä markkinoinnissa ja hän osti vuonna 1846 oikeudet myös Murrayn patenttiin. Ensimmäisen tehtaansa Lawes perusti vuonna 1844.[38]
Käyttö akkuhappona
[muokkaa | muokkaa wikitekstiä]Rikkihappoa käytetään elektrolyyttiliuoksena muun muassa autoissa käytettävissä lyijyakuissa. Akun purkautuessa lyijyanodilla tapahtuu hapettuminen seuraavan puolireaktion mukaisesti:
Lyijydioksidista koostuvalla katodilla akun purkautuessa tapahtuu pelkistysreaktio, jonka puolireaktio on:
Akun purkautuessa tapahtuva kokonaisreaktio voidaan kirjoittaa muodossa:
- Pb(s) + PbO2(s) + 2 H2SO4(aq) → 2 PbSO4(s) + 2 H2O(l)
Akun purkautuessa elektrolyyttinä oleva rikkihappo laimenee veden määrän lisääntyessä. Tämä huomataan elektrolyyttinesteen tiheyden pienentymisenä, ja tiheyttä voidaan käyttää määritettäessä akun purkautumistilaa. Reaktio on sähkövirran avulla palautettavissa alkuperäiseen tilaansa. Tällöin katodilla syntyy lyijydioksidia ja anodilla lyijymetallia.[43]
Käyttö orgaanisen kemian synteeseissä
[muokkaa | muokkaa wikitekstiä]Väkevä rikkihappo tai vaihtoehtoisesti fosforihappo kykenee eliminoimaan alkoholeista hydroksyyliryhmän eli poistamaan alkoholien tunnusryhmän ja muodostamaan alkeenejä ja vettä. Rikkihappo luovuttaa alkoholimolekyylille protonin, jolloin alkoholi muuttuu karbokationiksi ja hydroksyyliryhmä irtoaa muodostaen vettä. Veden poistuessa hiiliatomien välille muodostuu kaksoissidos. Helpoiten dehydraatio tapahtuu tertiäärisille alkoholeille (noin 100 °C:n lämpötilassa) ja vaikeammin sekundäärisille ja primäärisille alkoholeille (primääriset alkoholit vaativat noin 200 °C dehydratoituakseen).[44][45] Esimerkissä etanolin dehydraatio, jonka lopputuote on eteeni:
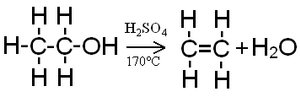
Esterisynteesissä rikkihapolla on kaksi tehtävää. Se toimii happamana katalyyttinä ja veden poistajana. Rikkihappo luovuttaa protonin karboksyylihapolle, jolloin muodostuu positiivinen ioni, joka reagoi helposti nukleofiilisen alkoholimolekyylin kanssa. Syntyvä välituote luovuttaa protonin, ja rakenteesta lohkeaa vesimolekyyli, jolloin syntyy esteri.[46] Esterisynteesi on tasapainoreaktio. Väkevä rikkihappo kykenee sitomaan itseensä vettä, jolloin esterisynteesin tasapaino siirtyy oikealle eli reaktiotuotteiden puolelle ja esterin saanto paranee.[47] Esimerkkinä etanolin ja etaanihapon reaktio, jossa syntyy etyyliasetaattia:

Rikkihappo toimii katalyyttinä niin ikään eetterisynteesissä, jossa se luovuttaa protonin alkoholimolekyylille, josta muodostuu karboniumioni. Karboniumioni reagoi toisen alkoholimolekyylin kanssa muodostaen eetterin. Eetterisynteesissä sivutuotteena voi syntyä rikkihapon hiilivetyjohdannaisia.[48]
Rikkihappo ympäristössä
[muokkaa | muokkaa wikitekstiä]Maapallolla
[muokkaa | muokkaa wikitekstiä]
Rikkihappoa syntyy ilmakehässä palokaasujen reaktioissa ja vulkaanisissa purkauksissa. Maapallon suurin rikkihappojärvi on 212 metriä syvä ja sijaitsee tulivuori Kawah Ijenin kraatterissa Indonesiassa. Pienempiä vulkaanisia rikkihappojärviä on muun muassa tulivuorilla Kusatsu-Shirane Japanissa ja Poás Costa Ricassa.[49]

Rikkihappo on typpihapon ohella yksi tärkeimmistä happosateiden ja happamoitumisen aiheuttajista. Polttoaineiden epäpuhtauksista joutuu ilmakehään rikkiä, joka hapettuu rikkidioksidiksi. Kuivassa ilmassa suurin osa rikkidioksidista varisee kuivalaskeumana maahan, pieni osa hapettuu rikkihapoksi. Jos ilmassa on vesipisaroita: pilviä, sumua tai sadepisaroita, rikkidioksidi voi hapettua nestefaasissa.[50] Reaktiot ilmakehässä kestävät yleensä muutamia päiviä, jonka aikana ilmakehän rikki on ehtinyt kulkeutua jopa sadankin kilometrin päähän. Sen vuoksi rikkipäästöjen vaikutukset, kuten joidenkin eliöryhmien lähes täydellinen puuttuminen, eivät välttämättä näy rikkiä vapauttavan kohteen ympäristössä. Happosateet nopeuttavat myös rakennusten ynnä muiden rakennelmien rapautumista, koska esimerkiksi muurilaasti ja rappaus sisältävät happojen kanssa herkästi reagoivaa kalsiumkarbonaattia.[51][52]
Happosateet olivat 1980-luvulle asti suuri ongelma Euroopan teollistuneilla alueilla, kuten Englannissa ja Ruhrin alueella Saksassa, missä poltettiin paljon rikkipitoista hiiltä. Näillä alueilla rikkipäästöt saatiin kuriin, ja Euroopan rikkidioksidipäästöt pienenivät puoleen vuosina 1980–1995. Samoin Yhdysvalloissa päästöt ovat vähentyneet voimakkaasti, muun muassa rikkipäästöjä säätelevän Clean Air Act -lain ansiosta. Ongelma on edelleen ajankohtainen Kiinassa, Koreassa, Venäjällä ja Itä-Euroopassa.[53] Liikenteen rikkipäästöt ovat vähentyneet, kun on siirrytty käyttämään vähärikkisempiä polttoaineita.[54] Suomen rikkilaskeuma on pienentynyt, mutta happamoituminen näkyy edelleen herkimmillä alueilla.[55]
Ilmakehän rikkihappomolekyyleillä on huomattava vaikutus pienhiukkasten syntymiseen. Ilmakehän rikkihappomolekyylikonsentraatio vaikuttaa merkittävästi hiukkasten nukleaatioon. Prosessin mekanismi ei ole vielä tarkoin selvillä, mutta rikkihapon vaikutus on tutkimuksien mukaan suurempi kuin esimerkiksi ammoniakin tai eräiden orgaanisten yhdisteiden. Rikkihappopitoisuuden ja hiukkasten muodostumisnopeuden välinen riippuvuus on pitkään ollut epäselvä. Helsingin yliopiston ja Ilmatieteen laitoksen tutkijoiden johtama ryhmä julkaisi vuonna 2010 tutkimuksen, jossa ensimmäisen kerran pystyttiin selvittämään rikkihapon määrän ja pienhiukkasten muodostumisnopeuksien välisiä riippuvuuksia.[56][57]
Venuksessa
[muokkaa | muokkaa wikitekstiä]
Maan ulkopuolella rikkihappoa on havaittu Venuksessa ja mahdollisesti Jupiterin Europa-kuussa. Venuksen rikkihappo syntyy hiilidioksidin, veden ja rikkidioksidin valokemiallisessa reaktiossa. Venuksen kaasukehästä suurin osa on hiilidioksidia. Ensimmäisessä vaiheessa Venuksen kaasukehään tunkeutuva aallonpituudeltaan alle 169 nanometrin ultraviolettisäteily hajottaa hiilidioksidin hiilimonoksidiksi ja voimakkaasti reagoivaksi atomaariseksi hapeksi. Happi reagoi rikkidioksidin kanssa, jota löytyy runsaasti Venuksen kaasukehän pilvistä, muodostaen rikkitrioksidia, joka veden kanssa muodostaa lopulta rikkihappoa.[58] Kokonaisreaktio voidaan siis ilmoittaa seuraavasti:
- CO2 → CO + O
- SO2 + O → SO3
- SO3 + H2O → H2SO4
Rikkihappo muodostaa paksuja pilviä noin 45–70 kilometrin korkeuteen Venuksen pinnasta. Pilvet ovat niin paksuja, ettei valo pysty läpäisemään niitä, ja siksi Venuksen pintaa ei voida havainnoida tavallisilla optisilla kaukoputkilla. Rikkihappo varautuu helposti, minkä vuoksi Venuksen kaasukehässä salamoi usein.[58] Rikkihapon sataessa pisarat eivät saavuta Venuksen pintaa. Aluksi pisaroiden vesi haihtuu, ja pisaran saavutettua kaasukehän alemman osan on lämpötila niin korkea, että rikkihappo hajoaa rikkitrioksidiksi ja vedeksi, joista rikkitrioksidi hajoaa nopeasti hapeksi ja rikkidioksidiksi. Happi reagoi kaasukehän hiilimonoksidin kanssa muodostaen hiilidioksidia.[59]
Katso myös
[muokkaa | muokkaa wikitekstiä]- Ditionihappo (H2S2O6)
- Fluoririkkihappo (HSO3F)
- Klooririkkihappo (HSO3Cl)
- Peroksirikkihappo (H2SO5)
- Peroksidirikkihappo (H2S2O8)
- Tiorikkihappo (H2S2O3)
Lähteet
[muokkaa | muokkaa wikitekstiä]- Rikkihapon kansainvälinen kemikaalikortti
- Rikkihapon ominaisuuksia Lukion kemian demonstraatioita
- Wiberg, Egon & Wiberg, Nils & Holleman, Arnold Frederick: Inorganic chemistry. Academic Press, 2001. ISBN 978-0-12-352651-9 Kirja Googlen teoshaussa. (englanniksi)
- Shakhashiri, Bassam Z.: Sulfuric acid scifun.chem.wisc.edu. (englanniksi)
- Onnettomuuden vaaraa aiheuttavat aineet: Rikkihappo 8.12.2008. Työterveyslaitos. Viitattu 28.11.2009.
- Kutney, Gerald: Sulfur, s. 36. ChemTec Publishing, 2007. ISBN 978-1-895198-37-9 Kirja Googlen teoshaussa (viitattu 16.6.2009). (englanniksi)
- Happamoituminen (Kemian tutkimuksia) Matemaattisten aineiden opetuksen tutkimus- ja kehittämiskeskus. Viitattu 28.11.2009.
- Pradyot Patnaik: Handbook of inorganic chemicals. McGraw-Hill Professional, 2002. ISBN 9780070494398 Kirja Googlen teoshaussa. (englanniksi)
- Derry, Thomas Kingston & Williams, Trevor Illtyd: A Short History of Technology. Courier Dover Publications, 1993. ISBN 0486274721 Kirja Googlen teoshaussa. (englanniksi)
- Yost, Don M.: Systematic Inorganic Chemistry. READ BOOKS, 2007. ISBN 1406773026 Kirja Googlen teoshaussa. (englanniksi)
- Louie, Douglas K.: Handbook of Sulfuric Acid Manufacturing. DKL Engineering, Inc, 2005. ISBN 978-0-9738992-0-7 Kirja Googlen teoshaussa. (englanniksi)
- Johnson, A. William: Invitation to Organic Chemistry. Jones & Bartlett Publishers, 1998. ISBN 9780763704322 Kirja Googlen teoshaussa. (englanniksi)
- Alexander, Elliot R.: Principles of Ionic Organic Reactions. READ BOOKS, 2007. ISBN 9781406746686 Kirja Googlen teoshaussa. (englanniksi)
- MyersMyers, Richard L.: The 100 Most Important Chemical Compounds: A Reference Guide. Greenwood Press, 2007. ISBN 9780313337581 Kirja Googlen teoshaussa. (englanniksi)
- McKetta, John J. & Weismantel, Guy E.: Encyclopedia of Chemical Processing and Design. CRC Press, 1999. ISBN 9780824726188 Kirja Googlen teoshaussa. (englanniksi)
Viitteet
[muokkaa | muokkaa wikitekstiä]- ↑ Rikkihapon kansainvälinen kemikaalikortti
- ↑ Sulfuric acid Encyclopedia Britannica. Viitattu 24.6.2009. (englanniksi)
- ↑ a b c Sulfuric acid SRI Consulting CEH Report: Sulfuric acid. Viitattu 29.6.2009. (englanniksi)
- ↑ a b 100 Most important Chemical compounds, s. 271
- ↑ a b Brian Shmaefsky: Favorite demonstrations for college science, s. 109. NSTA Press, 2004. ISBN 978-087-355-242-4 (englanniksi)
- ↑ Hydrogen Element Facts Chemicool. Viitattu 29.11.2009. (englanniksi)
- ↑ David M. Kiefer: Sulfuric acid: Pumping up the volume ACS Publications. Viitattu 29.11.2009. (englanniksi)
- ↑ Chenier, Philip J.: Survey of Industrial Chemistry, s. 45–57. John Wiley & Sons, New York, 1987. ISBN 978-156081622-5 (englanniksi)
- ↑ a b c Ova-ohje: Rikkihappo Työterveyslaitos. Viitattu 24.7.2009.
- ↑ Rikkihappo Ketsu
- ↑ Rikkihapon ominaisuuksia Lukion kemian demonstraatioita
- ↑ Seppänen, Raimo et al.: Maol-taulukot, s. 79. Otava, 2005 (2. painos). ISBN 9511206079
- ↑ Thomas Scott & Mary Eagleson: Concise encyclopedia chemistry, s. 1053. Walter de Gruyter, 1994. ISBN 978-311-011-451-5 (englanniksi)
- ↑ Gershon J. Shugar & Jack T. Ballinger & Linda M. Dawkins: Chemical technicians' ready reference handbook, s. 504. McGraw-Hill Professional, 1996. ISBN 9780070571860 Kirja Googlen teoshaussa. (englanniksi)
- ↑ Gupta, Ram B.: Hydrogen fuel: production, transport, and storage, s. 138. CRC Press, 2008. ISBN 9781420045758 Kirja Googlen teoshaussa. (englanniksi)
- ↑ Wiberg & Wiberg & Holleman, s. 547
- ↑ Happojen syövyttävyys Kemian opetuksen keskus. Viitattu 29.11.2009.
- ↑ a b Wiberg & Wiberg & Holleman, s. 548
- ↑ Patnaik, s. 456
- ↑ Drying, Chlorine Gas Krebs Swiss. Viitattu 29.11.2009. (englanniksi)
- ↑ Steven S. Zumdahl & Susan A. Zumdahl: Chemistry, s. 963. (8. painos) Brooks Cole. ISBN 978-0-495-82992-8 (englanniksi)
- ↑ Shakhashiri, Bassam Z.: Chemical demonstrations, s. 78–79. (ISBN 0299119505) University of Wisconsin Press, 1983. Kirja Googlen teoshaussa. (englanniksi)
- ↑ Kuvassa koko maailman tuotanto vuonna 1980 on arvioitu vuosien 1970 ja 1990 keskiarvosta.
- ↑ a b c Bassam Z. Shakhashiri: Sulfuric acid scifun.chem.wisc.edu. Viitattu 13.6.2009. (englanniksi)
- ↑ Gordon Graff: Sulfuric acid is suddenly scarce and expensive 13.9.2007. www.purchasing.com. Viitattu 22.7.2009. (englanniksi)
- ↑ Hannon, David: Sulfuric acid prices explode www.purchasing.com. Viitattu 22.7.2009. (englanniksi)
- ↑ Gordon Graff: Sulfuric Acid Price Bubble Bursts as Demand Softens www.soyatech.com. 22.12.2008. Viitattu 22.7.2009. (englanniksi)
- ↑ Outotec to deliver the world's largest sulfuric acid production facility to Saudi Arabia Sulfuric acid today. 25.2.2007. www.h2so4today.com. Viitattu 22.7.2009. (englanniksi)
- ↑ a b 100 Most important Chemical compounds, s. 272
- ↑ a b A Short History of Technology, s. 535
- ↑ a b Systematic Inorganic Chemistry, s. 333–335
- ↑ a b The Contact Process ChemGuide. Viitattu 30.6.2009. (englanniksi)
- ↑ Handbook of Sulfuric Acid Manufacturing
- ↑ McKetta & Weismantel, s. 144–151
- ↑ Marko Hamilo: Rikki haisee ja maistuu – yleensä pahalta 17.4.2007. Helsingin Sanomat. Viitattu 25.7.2009.
- ↑ Onnettomuuden vaaraa aiheuttavat aineet, Työterveyslaitos: Rikkihappo
- ↑ E513 - Rikkihappo Ruokavirasto. Viitattu 25.9.2023.
- ↑ a b c Kutney, Gerald: Sulfur, s. 36. Määritä julkaisija!
- ↑ Handbook of Silicon Wafer Cleaning Technology, s. 211–212. William Andrew, 2007. Teoksen verkkoversio. (englanniksi)
- ↑ OVA-ohje: rikkihappo Työterveyslaitos. Viitattu 29.11.2009.
- ↑ IFDC focuses on fertilizers and food security, Issue 4; Global Shortage of Sulfuric Acid Contributes to Rising Fertilizer Costs 2008. IFDC. Viitattu 28.7.2009. (englanniksi)
- ↑ Patnaik, s. 44
- ↑ Lead-Acid Battery Half-Cell Reactions Av8n.com. Viitattu 30.7.2009. (englanniksi)
- ↑ Johnson, s. 209
- ↑ Nevalainen, Tapio: 8.6 Alkoholien reaktiot Kuopion yliopisto. Viitattu 7.7.2009.
- ↑ Johnson, s. 557
- ↑ 9.3 The acidic environment: 5. Esterification Charles Sturt University. Viitattu 7.7.2009. (englanniksi)
- ↑ Alexander, s. 214
- ↑ Anitei, Stephan: The Largest Lake of Acid on Earth 21.3.2008. softpedia.com. Viitattu 30.7.2009. (englanniksi)
- ↑ Happamoituminen
- ↑ Acid Rain Factfile Science For All. Viitattu 29.11.2009. (englanniksi)
- ↑ Martínez-Ramírez S. & Thompson, G. E.: Wet deposition studies of hydraulic mortar. Materials and Structures, 1999, 32. vsk, nro 8, s. 606–610. Springer. ISSN 1359-5997 (Print) 1871-6873 (Online) Artikkelin verkkoversio. Viitattu 29.11.2009. (englanniksi)
- ↑ Vartia P.: Talouden ilmiöitä – teemana globalisaatio, s. 34. (ISBN 978-951-628-464-7) Helsinki: Taloudellinen Tiedotustoimisto, 2007. Teoksen verkkoversio.
- ↑ Bensiinin energia- ja päästöominaisuudet ja ympäristövaikutukset Motiva. Viitattu 20.6.2009.
- ↑ Metsien elinkykyyn kiinnitetään huomiota Suomella on raskas ekologinen jalanjälki, Tilastokeskus
- ↑ Ilmakehän pienhiukkasten syntymisestä uutta tietoa: rikkihappomysteeri ratkaistu Ilmatieteen laitos. Viitattu 6.3.2010.
- ↑ Sipilä et al.: The Role of Sulfuric Acid in Atmospheric Nucleation. Science, 5.3.2010, 327. vsk, nro 5970, s. 1243–1246. Artikkelin abstrakti. Viitattu 6.3.2010. (englanniksi)
- ↑ a b Acid clouds and lightning ESA. Viitattu 13.7.2009. (englanniksi)
- ↑ Rain and lightning Belgian Institute for Space Aeronomy. Viitattu 29.11.2009. (englanniksi)
Aiheesta muualla
[muokkaa | muokkaa wikitekstiä]- Rikkihappon kansainvälinen kemikaalikortti
- Kemian työsuojeluneuvottelukunta (KETSU): Rikkihappo
- Kyoto Encyclopedia of Genes and Genomes (KEGG): Sulfuric acid (englanniksi)
- Bristol University School of Chemistry, Molecule of the Month: Sulfuric acid (englanniksi)

