Antagonis dopamin
| antagonis reseptor dopamin Penyekat dopaminergik | |
|---|---|
| Kelas obat-obatan | |
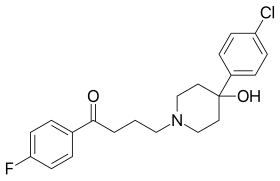 Rumus struktur rangka Haloperidol, suatu antipsikotik tipikal | |
| Pengenal kelas | |
| Penggunaan | Skizofrenia, gangguan bipolar, mual dan muntah, dll |
| Kode ATC | N05A |
| Target biologis | Reseptor dopamin |
| Pranala luar | |
| MeSH | D012559 |
| Dalam Wikidata | |
Antagonis dopamin, juga dikenal sebagai antidopaminergik dan antagonis reseptor dopamin (DRA), adalah jenis obat yang memblokir reseptor dopamin melalui antagonisme reseptor. Sebagian besar antipsikotik adalah antagonis dopamin, dan karenanya telah digunakan dalam mengobati skizofrenia, gangguan bipolar, dan psikosis stimulan.[1] Beberapa antagonis dopamin lainnya adalah antiemetik yang digunakan dalam pengobatan mual dan muntah.
Farmakologi reseptor
[sunting | sunting sumber]
Semua reseptor dopamin adalah reseptor yang terhubung dengan protein G, dan dibagi menjadi dua kelas berdasarkan protein G tempat reseptor tersebut terhubung. Kelas reseptor dopamin seperti D1 terhubung dengan Gαs/olf dan merangsang produksi adenilat siklase, sedangkan kelas seperti D2 terhubung dengan Gαi/o dan dengan demikian menghambat produksi adenilat siklase.[1]
Reseptor seperti D1: D1 dan D5
[sunting | sunting sumber]Reseptor seperti D1 – D1 dan D5 selalu ditemukan di pascasinaps. Gen yang mengkode reseptor ini tidak memiliki intron, jadi tidak ada varian sambatan.
Reseptor D1
[sunting | sunting sumber]- Reseptor D1 ditemukan terutama pada neuron di nukleus akumbens[2] serta substansia nigra, striatum, amigdala, korteks frontal, bulbus olfaktorius, dan retina[1]
- Reseptor ini juga ditemukan (dalam kadar yang lebih rendah) di hipotalamus, talamus, serebelum, dan hipokampus[1]
- Secara perifer reseptor ini ditemukan di arteri ginjal, arteri mesenterika, dan arteri limpa yang aktivasinya menyebabkan vasodilatasi. Selain itu, reseptor D1 ditemukan di ginjal[3]
Reseptor D5
[sunting | sunting sumber]- Kadar reseptor D5 yang rendah ditemukan di hipotalamus, korteks prefrontal, dan korteks cingulata; serta area memori seperti hipokampus, girus dentata, dan korteks entorinal.[1]
- Selain itu, reseptor D5 telah ditemukan di ginjal[3]
Reseptor mirip D2: D2, D3, dan D4
[sunting | sunting sumber]Reseptor mirip D2 tidak seperti kelas mirip D1, reseptor ini ditemukan sebelum dan sesudah sinapsis. Gen yang mengkode reseptor ini memiliki intron, yang menghasilkan banyak varian yang disambung secara bergantian.
Reseptor D2
[sunting | sunting sumber]- Reseptor D2 ditemukan di striatum, substantia nigra, area tegmental ventral, hipotalamus, korteks, septum, amigdala, hipokampus, dan tuberkulum olfaktorius.[1]
- Reseptor ini juga telah ditemukan di retina dan kelenjar pituitari.[1]
- Di bagian perifer, reseptor ini telah ditemukan di arteri renalis, mesenterika, dan limpa; serta di korteks dan medula adrenal dan di dalam ginjal.[3]
Reseptor D3
[sunting | sunting sumber]- Reseptor D3 banyak diekspresikan pada neuron di pulau Calleja dan cangkang nukleus akumbens dan sedikit diekspresikan di area seperti substantia nigra pars kompakta, hipokampus, area septum, dan area tegmental ventral.[1][2]
- Penelitian tambahan menemukan reseptor ini di bagian perifer ginjal[3]
Reseptor D4
[sunting | sunting sumber]Reseptor D4 ditemukan di amigdala, hipokampus, hipotalamus, globus palidus, substantia nigra pars retikula, talamus, retina, dan ginjal[1][3]
Implikasi pada penyakit
[sunting | sunting sumber]Sistem dopaminergik telah terlibat dalam berbagai gangguan. Penyakit Parkinson disebabkan oleh hilangnya neuron dopaminergik di striatum.[1] Lebih jauh lagi, antipsikotik yang paling efektif memblokir reseptor D2, yang menunjukkan peran dopamin dalam skizofrenia.[1][4][3] Studi tambahan berhipotesis bahwa disregulasi dopamin terlibat dalam penyakit Huntington, ADHD, sindrom Tourette, depresi mayor, depresi manik, kecanduan, hipertensi, dan disfungsi ginjal.[1][3][5] Antagonis reseptor dopamin digunakan untuk beberapa penyakit seperti skizofrenia, gangguan bipolar, mual, dan muntah.[1]
- Melatonin menekan aktivitas dopamin[6] sebagai bagian dari fungsi ritme sirkadian normal, meskipun ketidakseimbangan patologis telah terlibat dalam penyakit Parkinson[7]
Efek samping
[sunting | sunting sumber]Gejala-gejala tersebut dapat mencakup satu atau beberapa hal berikut dan berlangsung tanpa batas waktu bahkan setelah penghentian antagonis dopamin, terutama setelah penggunaan jangka panjang atau dosis tinggi:

- Gejala ekstrapiramidal (EPS) yang terkait dengan antipsikotik tipikal:
- Tahap awal – terjadi pada awal pengobatan atau setelah peningkatan dosis, pasien pulih ketika dosis diturunkan[10]
- Distonia akut[10] – spasmofili otot dan postur abnormal yang berkelanjutan, dan timbul dalam beberapa hari; dapat diobati dengan antikolinergik
- Faktor risiko meliputi usia, jenis kelamin, dan riwayat keluarga[10]
- Akatisia[10][3] - mondar-mandir dan gelisah dan timbul dalam beberapa bulan pertama; dapat diobati dengan penyekat beta dan benzodiazepin
- Parkinsonisme akibat efek pada jalur nigrostriatal[10][3] - meliputi tremor, bradikinesia, dan kekakuan otot
- faktor risiko meliputi usia dan jenis kelamin[10]
- Distonia akut[10] – spasmofili otot dan postur abnormal yang berkelanjutan, dan timbul dalam beberapa hari; dapat diobati dengan antikolinergik
- Tahap akhir – terjadi setelah pengobatan yang lama (berbulan-tahunan), gejala tetap ada bahkan setelah dosis diturunkan[10]
- Dihipotesiskan bahwa efek ini disebabkan oleh blokade kronis reseptor D2[3]
- Tahap awal – terjadi pada awal pengobatan atau setelah peningkatan dosis, pasien pulih ketika dosis diturunkan[10]
- Hiperprolaktinemia akibat blokade reseptor D2 di hipofisis anterior yang menyebabkan peningkatan pelepasan prolaktin.[8][11]
- Peningkatan nafsu makan termasuk peningkatan keinginan dan makan berlebihan yang menyebabkan penambahan berat badan[8][12][13]
- Peningkatan risiko penolakan insulin[12]
- Disfungsi seksual[8][9]
- Metabolisme perubahan dengan peningkatan risiko obesitas dan diabetes melitus tipe 2[8][12]
- Sedasi[8][9]
- Sindrom Neuroleptik Maligna, yakni keadaan darurat medis yang disebabkan oleh penurunan aktivitas dopaminergik, yang mengakibatkan blokade reseptor D2 sentral.[14]
Contoh
[sunting | sunting sumber]Antipsikotik generasi pertama (tipikal)
[sunting | sunting sumber]Antipsikotik generasi pertama digunakan untuk mengobati skizofrenia dan sering disertai dengan efek samping ekstrapiramidal.[1] Antipsikotik ini menghambat neurotransmisi dopaminergik di otak dengan memblokir sekitar 72% reseptor dopamin D2. Antipsikotik ini juga dapat memblokir aktivitas noradrenergik, kolinergik, dan histaminergik.[15]
- Benperidol[1] mengikat D2 dan beberapa reseptor serotonin. Antipsikotik ini diserap dengan sangat mudah dan memiliki efek lintas pertama yang tinggi.[16]
- Klorpromazin mengikat D3 dengan afinitas tertinggi, tetapi juga mengikat D1, D2, D4, dan D5[2][3]

- Klopentiksol[1]
- Droperidol digunakan sebagai antipsikotik dan antiemetik.[1]
- Haloperidol mengikat D2, D3, dan D4 dengan afinitas tertinggi, tetapi juga mengikat D1 dan D5.[1][2][3] Haloperidol juga berisiko memperpanjang QTc.[17]
- Flufenazin mengikat D2 dan D3 dengan afinitas tertinggi tetapi juga D1 dan D5[1][2]
- Flupentiksol mengikat D1, D2, D3, dan D5;[2] serta juga digunakan sebagai antidepresan.[1]
- Fluspirilen[1]
- Penfluridol[1]
- Perazin[1]
- Perfenazin[1]
- Pimozid mengikat D2 dan D3 dengan afinitas tinggi, juga mengikat reseptor D4[1][2]
- Spiperon mengikat D2, D3, dan D4 dengan afinitas tinggi; juga dapat mengikat D1[1][2]
- Sulpirid mengikat D2 dan D3[1][2] dan juga digunakan sebagai antidepresan.[1]
- Tioridazin mengikat D2, D3 dan D4 dengan afinitas tinggi; juga dapat mengikat D1 dan D5 pada konsentrasi yang lebih tinggi[2] Tioridazin memiliki risiko tertinggi terkait perpanjangan QTc di antara neuroleptik.[17]
Antipsikotik generasi kedua (atipikal)
[sunting | sunting sumber]Obat-obatan ini tidak hanya antagonis dopamin pada reseptor yang ditentukan, tetapi juga bekerja pada reseptor serotonin 5HT2A..[15][1] Obat-obatan ini memiliki lebih sedikit efek samping ekstrapiramidal dan lebih kecil kemungkinannya memengaruhi kadar prolaktin jika dibandingkan dengan antipsikotik tipikal.[11]
- Amisulprid mengikat D2 dan D3[2] dan digunakan sebagai antipsikotik, antidepresan, dan juga mengobati gangguan bipolar.[1] Obat ini mengobati gejala positif dan negatif dari skizofrenia.[13]
- Asenapin mengikat D2, D3, dan D4[18]; digunakan untuk mengobati gangguan bipolar dan skizofrenia.[19] Efek sampingnya meliputi penambahan berat badan, tetapi risiko hipotensi ortostatik dan hiperprolaktinemia lebih rendah.
- Aripiprazol mengikat D2 sebagai agonis parsial, tetapi menghambat D3.[20] Selain itu aripiprazol mengobati skizofrenia, gangguan bipolar (mania),[21] depresi,[1] dan gangguan tic[20]

- Klozapin mengikat D1 dan D4 dengan afinitas tertinggi tetapi masih mengikat D2 dan D3.[2] Klozapin unik karena hanya diresepkan ketika pengobatan dengan setidaknya dua antipsikotik lain telah gagal karena efek sampingnya yang sangat keras. Obat ini juga memerlukan hitung sel darah putih mingguan untuk memantau potensi neutropenia.[13]
- Loksapin mengikat D2, D3 dan D4 dengan afinitas tinggi; juga dapat mengikat D1.[22] Loksapin sering digunakan untuk mengobati pasien yang gelisah dan kasar dengan gangguan neuropsikiatri seperti gangguan bipolar dan skizofrenia.[23]
- Nemonaprid mengikat D3, D4 dan D5.[3]
- Olanzapin mengikat semua reseptor[2] dan digunakan untuk mengobati gejala positif dan negatif skizofrenia serta gangguan bipolar dan depresi.[1] Obat ini dikaitkan dengan penambahan berat badan yang signifikan.[13]
- Kuetiapin mengikat D1, D2 dan D3; serta dapat mengikat D4 pada konsentrasi tinggi.[2] Obat ini digunakan untuk mengobati gejala positif skizofrenia,[13] gangguan bipolar, dan depresi.[1] Dari antipsikotik generasi kedua, kuetiapin dapat menghasilkan lebih sedikit efek samping parkinson.[24]
- Paliperidon mengikat D2, D3 dan D4 dengan afinitas tinggi; juga dapat mengikat D1 dan D5.[25]
- Remoksiprid mengikat reseptor D2 dengan afinitas yang relatif rendah.[2][11][1]
- Risperidon mengikat reseptor D2, D3 dan D4.[1][2][25] Risperidon tidak hanya mengobati gejala positif dan negatif skizofrenia[13] tetapi juga mengobati gangguan bipolar.[1]
- Tiaprid menghambat D2 dan D3 dan digunakan sebagai antipsikotik.[1] Obat ini juga sering digunakan untuk mengobati diskinesia, agitasi psikomotor, tic, korea Huntington, dan ketergantungan alkohol.[26]
- Ziprasidon menghambat reseptor D2[27] dan digunakan untuk mengobati skizofrenia, depresi, dan gangguan bipolar.[1] Ada kontroversi mengenai apakah Ziprasidon mengobati gejala negatif dan obat ini memiliki efek samping gastrointestinal yang terdokumentasi dengan baik.[13] Ziprasidon juga dapat menyebabkan perpanjangan QTc.[17]
Antagonis dopamin yang digunakan untuk mengobati mual dan muntah
[sunting | sunting sumber]- Domperidon adalah antagonis reseptor dopamin D2 selektif perifer yang digunakan sebagai antiemetik, agen gastroprokinetik, dan galaktagog.
- Bromoprida mengikat reseptor D2 enterik[28] dan juga mengobati gastroparesis.[1]
- Metoklopramid juga mengobati gastroparesis[1]
Antagonis dopamin yang hanya digunakan dalam penelitian
[sunting | sunting sumber]- Etikloprida mengikat D2 dan D3 dengan afinitas tinggi tetapi juga mengikat D4[2][3][29]
- Nafadotrida mengikat D2 dan D3[1][2][3]
- Rakloprida mengikat D2 dan D3[1][2] dan dapat diberi label radioaktif, dan digunakan dalam pencitraan PET untuk mengidentifikasi perkembangan penyakit pada Penyakit Huntington[30]
Antagonis dopamin lainnya
[sunting | sunting sumber]- Mesdopetam sedang dikembangkan untuk mengatasi diskinesia dan psikosis yang disebabkan oleh levodopa pada orang dengan penyakit Parkinson[31][32][33]
Referensi
[sunting | sunting sumber]- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap Beaulieu JM, Gainetdinov RR (March 2011). "The physiology, signaling, and pharmacology of dopamine receptors". Pharmacological Reviews. 63 (1): 182–217. doi:10.1124/pr.110.002642. PMID 21303898.
- ^ a b c d e f g h i j k l m n o p q r s Sokoloff P, Diaz J, Le Foll B, Guillin O, Leriche L, Bezard E, Gross C (February 2006). "The dopamine D3 receptor: a therapeutic target for the treatment of neuropsychiatric disorders". CNS & Neurological Disorders Drug Targets. 5 (1): 25–43. doi:10.2174/187152706784111551. PMID 16613552.
- ^ a b c d e f g h i j k l m n o p Missale C, Nash SR, Robinson SW, Jaber M, Caron MG (January 1998). "Dopamine receptors: from structure to function". Physiological Reviews. 78 (1): 189–225. doi:10.1152/physrev.1998.78.1.189. PMID 9457173.
- ^ Seeman P (August 2006). "Targeting the dopamine D2 receptor in schizophrenia". Expert Opinion on Therapeutic Targets. 10 (4): 515–31. doi:10.1517/14728222.10.4.515. PMID 16848689.
- ^ Iversen SD, Iversen LL (May 2007). "Dopamine: 50 years in perspective". Trends in Neurosciences. 30 (5): 188–93. doi:10.1016/j.tins.2007.03.002. PMID 17368565.
- ^ Zisapel N (December 2001). "Melatonin-dopamine interactions: from basic neurochemistry to a clinical setting". Cellular and Molecular Neurobiology. 21 (6): 605–16. doi:10.1023/A:1015187601628. PMID 12043836.
- ^ Willis GL (2008). "Parkinson's disease as a neuroendocrine disorder of circadian function: dopamine-melatonin imbalance and the visual system in the genesis and progression of the degenerative process". Reviews in the Neurosciences. 19 (4–5): 245–316. doi:10.1515/revneuro.2008.19.4-5.245. PMID 19145986.
- ^ a b c d e f Young SL, Taylor M, Lawrie SM (April 2015). ""First do no harm." A systematic review of the prevalence and management of antipsychotic adverse effects". Journal of Psychopharmacology. 29 (4): 353–62. doi:10.1177/0269881114562090. PMID 25516373.
- ^ a b c Arana GW (2000). "An overview of side effects caused by typical antipsychotics". The Journal of Clinical Psychiatry. 61 (Suppl 8): 5–11; discussion 12–3. PMID 10811237.
- ^ a b c d e f g h i Divac N, Prostran M, Jakovcevski I, Cerovac N (2014). "Second-generation antipsychotics and extrapyramidal adverse effects". BioMed Research International. 2014: 656370. doi:10.1155/2014/656370
 . PMC 4065707
. PMC 4065707  . PMID 24995318.
. PMID 24995318.
- ^ a b c Nadal R (2001). "Pharmacology of the atypical antipsychotic remoxipride, a dopamine D2 receptor antagonist". CNS Drug Reviews. 7 (3): 265–82. doi:10.1111/j.1527-3458.2001.tb00199.x. PMC 6741677
 . PMID 11607043.
. PMID 11607043.
- ^ a b c Deng C (September 2013). "Effects of antipsychotic medications on appetite, weight, and insulin resistance". Endocrinology and Metabolism Clinics of North America. 42 (3): 545–63. doi:10.1016/j.ecl.2013.05.006. PMID 24011886.
- ^ a b c d e f g Mortimer AM (March 2004). "How do we choose between atypical antipsychotics? The advantages of amisulpride". The International Journal of Neuropsychopharmacology. 7 Suppl 1 (5): S21–5. doi:10.1017/S1461145704004134
 . PMID 14972081.
. PMID 14972081.
- ^ Berman, Brian (January 2011). "Neuroleptic Malignant Syndrome". The Neuro Hospitalists. 1 (1): 41–47. doi:10.1177/1941875210386491. PMC 3726098
 . PMID 23983836.
. PMID 23983836.
- ^ a b Chokhawala, Krutika (2 October 2021). "Antipsychotic Medications". StatPearls. PMID 30137788 – via NCBI.
- ^ Leucht S, Hartung B (April 2005). "Benperidol for schizophrenia". The Cochrane Database of Systematic Reviews. 2005 (2): CD003083. doi:10.1002/14651858.CD003083.pub2. PMC 7017029
 . PMID 15846648.
. PMID 15846648.
- ^ a b c Beach, Scott (2013). "QTc prolongation, torsades de pointes, and psychotropic medications". The Academy of Psychosomatic Medicine. 54 (1): 1–13. doi:10.1016/j.psym.2012.11.001
 . PMID 23295003.
. PMID 23295003.
- ^ Stoner SC, Pace HA (May 2012). "Asenapine: a clinical review of a second-generation antipsychotic". Clinical Therapeutics. 34 (5): 1023–40. doi:10.1016/j.clinthera.2012.03.002. PMID 22494521.
- ^ Scheidemantel T, Korobkova I, Rej S, Sajatovic M (2015-12-04). "Asenapine for bipolar disorder". Neuropsychiatric Disease and Treatment. 11: 3007–17. doi:10.2147/NDT.S78043
 . PMC 4675633
. PMC 4675633  . PMID 26674884.
. PMID 26674884.
- ^ a b Yang CS, Huang H, Zhang LL, Zhu CR, Guo Q (July 2015). "Aripiprazole for the treatment of tic disorders in children: a systematic review and meta-analysis". BMC Psychiatry. 15: 179. doi:10.1186/s12888-015-0504-z
 . PMC 4518630
. PMC 4518630  . PMID 26220447.
. PMID 26220447.
- ^ Brown R, Taylor MJ, Geddes J (December 2013). "Aripiprazole alone or in combination for acute mania" (PDF). The Cochrane Database of Systematic Reviews (12): CD005000. doi:10.1002/14651858.CD005000.pub2. PMC 11330668
 Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 24346956. - ^ Popovic D, Nuss P, Vieta E (2015-04-01). "Revisiting loxapine: a systematic review". Annals of General Psychiatry. 14: 15. doi:10.1186/s12991-015-0053-3
 . PMC 4391595
. PMC 4391595  . PMID 25859275.
. PMID 25859275.
- ^ Pollack CV (July 2016). "Inhaled loxapine for the urgent treatment of acute agitation associated with schizophrenia or bipolar disorder". Current Medical Research and Opinion. 32 (7): 1253–60. doi:10.1185/03007995.2016.1170004. PMID 27121764.
- ^ Asmal, Laila (2013). "Quetiapine versus other atypical antipsychotics for schizophrenia". Cochrane Database of Systematic Reviews (11): CD006625. doi:10.1002/14651858.CD006625.pub3. PMID 24249315.
- ^ a b Corena-McLeod M (June 2015). "Comparative Pharmacology of Risperidone and Paliperidone". Drugs in R&D. 15 (2): 163–74. doi:10.1007/s40268-015-0092-x. PMC 4488186
 . PMID 25943458.
. PMID 25943458.
- ^ Dose M, Lange HW (January 2000). "The benzamide tiapride: treatment of extrapyramidal motor and other clinical syndromes". Pharmacopsychiatry. 33 (1): 19–27. doi:10.1055/s-2000-7964. PMID 10721880.
- ^ Stahl SM, Shayegan DK (2003). "The psychopharmacology of ziprasidone: receptor-binding properties and real-world psychiatric practice". The Journal of Clinical Psychiatry. 64 (Suppl 19): 6–12. PMID 14728084.
- ^ Tonini M, Cipollina L, Poluzzi E, Crema F, Corazza GR, De Ponti F (February 2004). "Review article: clinical implications of enteric and central D2 receptor blockade by antidopaminergic gastrointestinal prokinetics". Alimentary Pharmacology & Therapeutics. 19 (4): 379–90. doi:10.1111/j.1365-2036.2004.01867.x
 . PMID 14871277.
. PMID 14871277.
- ^ Martelle JL, Nader MA (2008). "A review of the discovery, pharmacological characterization, and behavioral effects of the dopamine D2-like receptor antagonist eticlopride". CNS Neuroscience & Therapeutics. 14 (3): 248–62. doi:10.1111/j.1755-5949.2008.00047.x. PMC 2753830
 . PMID 18801115.
. PMID 18801115.
- ^ Pagano G, Niccolini F, Politis M (June 2016). "Current status of PET imaging in Huntington's disease". European Journal of Nuclear Medicine and Molecular Imaging. 43 (6): 1171–82. doi:10.1007/s00259-016-3324-6. PMC 4844650
 . PMID 26899245.
. PMID 26899245.
- ^ "Mesdopetam - Integrative Research Laboratories". AdisInsight. 6 September 2024. Diakses tanggal 25 September 2024.
- ^ Alsalmi M, Al-Kassmy J, Kang W, Palayew M, Huot P (2024). "Levodopa-induced dyskinesia: do current clinical trials hold hope for future treatment?". Expert Opin Pharmacother. 25 (1): 1–3. doi:10.1080/14656566.2023.2298345
 . PMID 38116733 Periksa nilai
. PMID 38116733 Periksa nilai |pmid=(bantuan). - ^ Kiss B, Laszlovszky I, Krámos B, Visegrády A, Bobok A, Lévay G, Lendvai B, Román V (January 2021). "Neuronal Dopamine D3 Receptors: Translational Implications for Preclinical Research and CNS Disorders". Biomolecules. 11 (1): 104. doi:10.3390/biom11010104
 . PMC 7830622
. PMC 7830622  . PMID 33466844 Periksa nilai
. PMID 33466844 Periksa nilai |pmid=(bantuan).
