Borna kiselina
| Borna kiselina | |||
|---|---|---|---|
 |
 | ||

| |||
| IUPAC ime |
| ||
| Identifikacija | |||
| CAS registarski broj | 10043-35-3 | ||
| PubChem[1][2] | 7628 | ||
| ChemSpider[3] | 7346 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | H3BO3 | ||
| Molarna masa | 61.83 g mol−1 | ||
| Agregatno stanje | Kristal bijele boje | ||
| Gustina | 1.435 g/cm3 | ||
| Tačka topljenja |
170.9 °C, 444 K, 340 °F | ||
| Tačka ključanja |
300 °C, 573 K, 572 °F | ||
| Rastvorljivost u vodi | 2.52 g/100 mL (0 °C) 4.72 g/100 mL (20 °C) 5.7 g/100 mL (25 °C) 19.10 g/100 mL (80 °C) 27.53 g/100 mL (100 °C) | ||
| Rastvorljivost u other solvents | Rastvorljiva u nižim alkoholima umjereno rastvorljiva u piridinu vrlo malo rastvorljiva u acetonu | ||
| pKa | 5.2 | ||
| Opasnost | |||
| NFPA 704 | |||
| Tačka paljenja | Nezapaljiva | ||
| LD50 | 2660 mg/kg, oralno (pacov) | ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | Bor trioksid Boraks | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
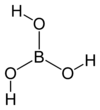
Borna kiselina (hemijska formula H3BO3 ili B(OH)3) je supstanca koja spada u slabe neorganske kiseline. Postoji u obliku bezbojnih kristala ili bijelog praha i rastvorljiva je u vodi. Može se naći i u mineralnom obliku i tada se naziva sasolit. U prirodi se može naći u nekim vulkanskim oblastima, u sastavu raznih minerala (npr. boraks), u morskoj vodi, u biljkama i voću.
Molekul borne kiseline B(OH)3 je planaran. Atom bora u molekulu borne kiseline je sp2 hibridizovan, tj. tri sp2 hibridne orbitale se nalaze u istoj ravni a ugao između njih je 120 °. Bor sa kiseonikom gradi kovalentne veze (posredstvom sp2 orbitala) i zbog toga je cijeli molekul planaran . Borna kiselina se u čvrstom stanju sastoji od slojeva B(OH)3 molekula koje na okupu drži vodonična veza. Rastojanje između dva susjedna sloja je 318 pm.
 |
 |
dovodi da molekuli borne kiseline formiraju paralelne slojeve u čvrstom stanju |
Borna kiselina se može dobiti u reakciji između boraksa i neke neorganske kiseline, kao npr. hlorovodonične kiseline:
- Na2B4O7·10H2O + 2 HCl → 4 B(OH)3 [or H3BO3] + 2 NaCl + 5 H2O
Borna kiselina je rastvorljiva u ključaloj vodi. Pri zagrijavanju iznad 170 °C dolazi do reakcije dehidratacije pri čemu nastaje borična kiselina (HBO2):
- H3BO3 → HBO2 + H2O
Borična kiselina je bijela, kristalna supstanca i djelimično je rastvorljiva u vodi. Topi se na 236 °C a pri zagrijavanju preko 300 °C dolazi do daljnje dehidratacije pri čemu se formira tetraborična kiselina ili piroborična kiselina:
- 4 HBO2 → H2B4O7 + H2O
Daljnjim zagrijavanjem dobija se bor(III)-oksid:
- H2B4O7 → 2 B2O3 + H2O
Borna kiselina disosuje u vodenom rastvoru:
- B(OH)3 + H2O
 B(OH)4- + H+ (Ka = 5.8x10−10 mol/l; pKa = 9.24)
B(OH)4- + H+ (Ka = 5.8x10−10 mol/l; pKa = 9.24)
Pri tome se borna kiselina ponaša kao Luisova kiselina, tj. reaguje sa molekulom vode i prima elektronski par od OH- grupe, što je čini kiselinom po Luisovoj teoriji. Nagrađeni B(OH)4- jon ima tetraedarski oblik, tj. tetraedarski raspored atomskih grupa oko atoma bora.
U rastvorima sa pH vrijednošću 7-10, i ako je koncentracija bora veća od 0.025 mol/L dolazi do stvaranja poliboratnih jona. Najpoznatiji je tetraboratni jon koji se nalazi u mineralu boraksu:
- 4B(OH)4- + 2 H+
 B4O72- + 9 H2O
B4O72- + 9 H2O
Borna kiselina nalazi primjenu kao antiseptik, insekticid, za sprječavanje širenja vatre itd. U industriji nalazi primjenu u proizvodnji fiberglasa, za pravljenje sredstava za podmazivanje drveta. Koristi se i u pirotehnici.
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.

