Cystationín
| Cystationín | |
 | |
 | |
| Všeobecné vlastnosti | |
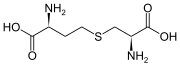
| Sumárny vzorec | C7H14N2O4S |
| Systematický názov | S-((R)-2-amino-2-karboxyetyl)-L-homocysteín |
| Fyzikálne vlastnosti | |
| Molárna hmotnosť | 222,26 g/mol |
| Ďalšie informácie | |
| Číslo CAS | 56-88-2 |
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |
Cystationín je aminokyselina, ktorá vzniká ako medziprodukt v syntéze cysteínu. Umožňuje prenos tiolovej skupiny z homocysteínu na cysteín alebo naopak.
Vznik
[upraviť | upraviť zdroj]Cystationín vzniká v transsulfuračnej ceste, ktorá premieňa homocysteín na cystationín. V tejto dráhe dochádza k spojeniu homocysteínu a serínu pomocou cystationín-β-syntázy.[1][2][3] Cystationín sa potom štiepi na α-ketobutyrát a cysteín pôsobením cystationín-γ-lyázy.[1][3] Takto prebieha prenos tiolovej skupiny u ľudí a zvierat.[3]

Celý proces môže prebiehať i opačným smerom. Cystationín môže vznikať opačným procesom, a to spojením cysteínu s aktivovaným homoserínom. Túto reakciu katalyzuje cystationín-γ-syntáza. Cystationín sa potom rozkladá na homocysteín, pyruvát a amoniak pôsobením cystationín-β-lyázy.[2][3] Týmto spôsobom prebieha transsulfurácia u rastlín a kvasiniek.[3]
Metabolické premeny
[upraviť | upraviť zdroj]Cystationín môže byť spracovávaný enzýmami cystationín-γ-lyázou, cysteíndioxygenázou a sulfinoalaníndekarboxylázou, čím z neho vzniká hypotaurín a taurín.[4]
Cysteín, ktorý vzniká pôsobením cystationín-γ-lyázy na cystationín, potom môže byť využitý i enzýmom glutamát-cysteínligázou a glutatiónsyntetázou, čím z neho vzniká glutatión.[1]
Patológia
[upraviť | upraviť zdroj]Nadbytok cystationínu v moči sa nazýva cystationínúria. Cystationínúria vzniká nedostatočnou aktivitou cystationín-γ-lyázy, čím dochádza k hromadeniu cystationínu v plazme.[5]
Referencie
[upraviť | upraviť zdroj]- ↑ a b c VOET, Donald. Biochemistry. Hoboken, NJ : John Wiley & Sons, 2011. (4th edition.) Dostupné online. ISBN 978-0-470-57095-1. S. 1036, 1061.
- ↑ a b Axis-Shield Liquid Stable (LS) 2-Part Homocysteine Assay [online]. [Cit. 2022-10-07]. Dostupné online.
- ↑ a b c d e CLAUSEN, Tim; HUBER, Robert; LABER, Bernd. Crystal Structure of the Pyridoxal-5′-phosphate Dependent Cystathionine β-lyase fromEscherichia coliat 1.83 Å. Journal of Molecular Biology, 1996-09-20, roč. 262, čís. 2, s. 202–224. Dostupné online [cit. 2022-10-07]. ISSN 0022-2836. DOI: 10.1006/jmbi.1996.0508. (po anglicky)
- ↑ Harris Ripps, Wen Shen. Review: Taurine: A "very essential" amino acid. Molecular Vision, 2012, s. 2673–2686. PMID 23170060.
- ↑ CYSTATHIONINURIA [online]. . Dostupné online.
Zdroj
[upraviť | upraviť zdroj]Tento článok je čiastočný alebo úplný preklad článku Cystathionine na anglickej Wikipédii.
