Foszfor-pentoxid
| Foszfor-pentoxid | |
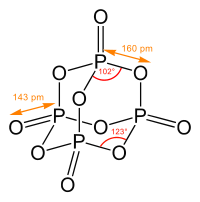 Foszfor-pentoxid | |
 Foszfor-pentoxid | |
| Más nevek | Foszfor(V)-oxid Difoszfor-pentaoxid, Foszforsavanhidrid |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | [1314-56-3] (P2O5) [16752-60-6] (P4O10) |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | P4O10 |
| Moláris tömeg | 283,889 g mol−1 |
| Megjelenés | fehér, higroszkópos por |
| Sűrűség | 2,30 g cm−3,[1] szilárd |
| Olvadáspont | 340-360 °C[1] |
| Forráspont | 591 °C[1] |
| Oldhatóság (vízben) | foszforsavra hidrolizál |
| Gőznyomás | 1,3 mbar 384 °C-on[1] |
| Veszélyek | |
| EU osztályozás | Maró (C)[1] |
| NFPA 704 | |
| R mondatok | R35[1] |
| S mondatok | (S1/2), S22, S26, S45[1] |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A foszfor-pentoxid (vagy difoszfor-pentaoxid, foszfor(V)-oxid, foszforsavanhidrid) a foszfor egyik oxidja, +5-ös oxidációs számú foszfort tartalmaz. Közönséges körülmények közt fehér színű, szilárd anyag. Ha hevítik, szublimál. Kétféle kristályos módosulata van, ezek közül a rombos szerkezetű kristályokat alkotó módosulat a stabilabb. Erősen higroszkópos vegyület. Vizet szív a levegőből. A foszforsav anhidridje.
Szerkezete
[szerkesztés]A foszfor-pentoxid gőzeiben P4O10 dimer molekulák találhatók. A gőz sűrűsége alapján is erre lehet következtetni. A dimer molekula szerkezete a difoszfor-trioxid molekuláéra emlékeztet, a két molekula szerkezete abban különbözik, hogy a foszfor-pentoxidban még egy-egy oxigénatom kapcsolódik minden foszforatomhoz. A foszforatomok koordinációs száma négy. A foszforatomok az öt vegyértékelektronjuk közül néggyel szigma-kötést létesítenek, az ötödikkel pi-kötést alkotnak a tetraéderek csúcsán található oxigénatomokkal, ennek a kötésnek a kötésrendje körülbelül 2. A foszforatomok illetve a tetraéderek csúcsain található oxigénatomok közti kötéstávolság (139 pm) sokkal rövidebb, mint a tetraéderek élein található oxigén-foszfor kötések kötéstávolsága (162 pm).
Kémiai tulajdonságai
[szerkesztés]A foszfor-pentoxid igen higroszkópos vegyület. Vízzel először sercegés közben metafoszforsavvá egyesül, a reakció nagy hőfejlődéssel jár. A képződő metafoszforsav további vizet vehet fel és ortofoszforsavvá alakulhat.
Előállítása
[szerkesztés]A foszfor-pentoxid akkor képződik, ha foszfort feleslegben lévő oxigénnel reagáltatnak.
A kereskedelmi foszfor-pentoxid gyakran kisebb oxidációs fokú foszfor-oxidokat is tartalmaz. Ezektől úgy szabadítják meg, hogy oxigénáramban szublimáltatják.
Felhasználása
[szerkesztés]Mivel erősen higroszkópos, szárítószerként alkalmazzák. Laboratóriumokban felhasználják gázok és folyadékok szárítására. Alkalmazzák még vízelvonáson alapuló reakcióknál, foszforsav és műtrágya előállítására.
Jegyzetek
[szerkesztés]- ↑ a b c d e f g A foszfor-pentoxid vegyülethez tartozó bejegyzés az IFA GESTIS adatbázisából. A hozzáférés dátuma: 2010. október 29. (JavaScript szükséges) (angolul)
- ↑ Dr. Rohonczy János. Szervetlen kémia I.. Budapest: Eötvös Lóránd Tudományegyetem Természettudományi Kar, 51. o. (2017). ISBN 978-963-284-853-2
Források
[szerkesztés]- Erdey-Grúz Tibor: Vegyszerismeret
- Nyilasi János Szervetlen kémia
- Bodor Endre: Szervetlen kémia I.




