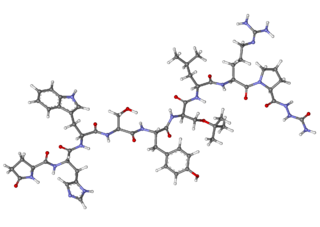
Goserelina
| Goserelina | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| N-(21-((1H-indol-3-yl)methyl)-1,1-diamino-12-(tert-butoxymethyl)-6-(2-(2-carbamoylhydrazinecarbonyl)cyclopentanecarbonyl)-15-(4-hydroxybenzyl)-18-(hydroxymethyl)-25-(1H-imidazol-5-yl)-9-isobutyl-8,11,14,17,20,23-hexaoxo-2,7,10,13,16,19,22-heptaazapentacos-1-en-24-yl)-5-oxopyrrolidine-2-carboxamide | ||
| Identificadores | ||
| Número CAS | 65807-02-5 | |
| Código ATC | L02AE03 | |
| PubChem | 5311128 | |
| DrugBank | DB00014 | |
| ChemSpider | 4470656 | |
| UNII | 0F65R8P09N | |
| KEGG | D04405 | |
| ChEBI | 5523 | |
| ChEMBL | 1201247 | |
| Datos químicos | ||
| Fórmula | C59H84N18O14 | |
| Peso mol. | 1269,410 g/mol | |
|
CC(C)C[C@H](NC(=O)[C@@H](COC(C)(C)C)NC(=O)[C@H](CC1=CC=C(O)C=C1)NC(=O)[C@H](CO)NC(=O)[C@H](CC1=CNC2=CC=CC=C12)NC(=O)[C@H](CC1=CN=CN1)NC(=O)[C@@H]1CCC(=O)N1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1CCC[C@H]1C(=O)NNC(N)=O
| ||
|
InChI=1S/C59H84N18O14/c1-31(2)22-40(49(82)68-39(12-8-20-64-57(60)61)56(89)77-21-9-13-46(77)55(88)75-76-58(62)90)69-54(87)45(29-91-59(3,4)5)74-50(83)41(23-32-14-16-35(79)17-15-32)70-53(86)44(28-78)73-51(84)42(24-33-26-65-37-11-7-6-10-36(33)37)71-52(85)43(25-34-27-63-30-66-34)72-48(81)38-18-19-47(80)67-38/h6-7,10-11,14-17,26-27,30-31,38-46,65,78-79H,8-9,12-13,18-25,28-29H2,1-5H3,(H,63,66)(H,67,80)(H,68,82)(H,69,87)(H,70,86)(H,71,85)(H,72,81)(H,73,84)(H,74,83)(H,75,88)(H4,60,61,64)(H3,62,76,90)/t38-,39-,40-,41-,42-,43-,44-,45+,46-/m0/s1
Key: BLCLNMBMMGCOAS-URPVMXJPSA-N | ||
| Farmacocinética | ||
| Unión proteica | 27,3% | |
| Vida media | 4-5 horas | |
| Excreción | Hepático | |
| Datos clínicos | ||
| Nombre comercial | Zoladex | |
| Cat. embarazo | D (3.6mg)/X(10.8mg) (USA) | |
| Estado legal | ℞-Receta requerida | |
| Vías de adm. | Implante | |
El acetato de goserelina (Zoladex, AstraZeneca[1]) es un análogo superagonista de la hormona liberadora de gonadotrofina (agonista GnRH), también conocido como un análogo agonista de la hormona liberadora de hormona luteinizante (LHRH).[2] Estructuralmente, es un decapéptido con estructura química piro-glu-his-trp-ser-tyr-D-ser(but)-leu-arg-pro-azgly-NH2. El acetato de goserelina se utiliza para suprimir la producción de las hormonas sexuales (testosterona y estrógeno), particularmente en el tratamiento de cáncer de mama y de próstata.
El acetato de goserelina estimula la producción de las hormonas sexuales testosterona y estrógeno en una manera no pulsante (no fisiológica). Esto provoca una interrupción en los sistemas de retroalimentación de las hormonas endógenas, resultando en una regulación a la baja de la producción de testosterona y estrógeno.
Zoladex fue aprobado por la FDA de Estados Unidos en 1989[3] para el tratamiento de cáncer de próstata.
Farmacocinética
[editar]La goserelina es un análogo sintético de una hormona natural liberadora de gonadotrofina (LHRH). La biodisponibilidad es casi completa. La goserelina tiene una unión proteica baja y tiene una vida media de eliminación sérica de dos a cuatro horas en pacientes con función renal normal. La vida media aumenta en pacientes con insuficiencia renal . No hay ningún cambio significativo en la farmacocinética en sujetos con insuficiencia hepática. Después de su administración, las concentraciones séricas máximas se alcanzan en aproximadamente dos horas. Se une rápidamente a las células del receptor de LHRH en la glándula pituitaria lo que conduce a un aumento inicial en la producción de la hormona luteinizante y lo que conduce a un aumento inicial en la producción de las correspondientes hormonas sexuales. Este brote inicial puede ser tratado con la coprescripción/coadministración de un antagonista del receptor androgénico tal como la bicalutamida. Finalmente, después de un período de aproximadamente 14-21 días, la producción de LH se reduce en gran medida debido a la regulación a la baja del receptor, y las hormonas sexuales son generalmente reducidas a niveles de castración.[4]
Indicaciones
[editar]
El acetato de goserelina se utiliza para tratar los cánceres hormona-sensibles de mama (en mujeres pre y peri menopáusicas) y de próstata, y algunos trastornos ginecológicos benignos (endometriosis, fibromas uterinos y adelgazamiento del endometrio). Además, la goserelina se utiliza en la reproducción asistida y en el tratamiento de la pubertad precoz. También se puede utilizar en el tratamiento de transexuales hombre-a-mujer[5] y es favorecida por encima de otros anti-andrógenos en algunos países, como el Reino Unido. Está disponible en implantes de 1 mes de duración y de acción prolongada con 3 meses de duración.
Desarrollo y Aprobaciones de la Goserelina
[editar]1. Desarrollo
[editar]- Fecha: La goserelina fue desarrollada a finales de la década de 1970.
- País: Reino Unido.
- Institución: Desarrollada por el laboratorio ICI Pharmaceuticals, ahora conocido como AstraZeneca.
- Investigadores Principales: El desarrollo de goserelina fue un esfuerzo colaborativo de un equipo de científicos e investigadores en ICI Pharmaceuticals. No se destaca a un solo individuo como inventor principal.
2. Aprobación por la FDA
[editar]- Fecha de Aprobación: La FDA (Administración de Alimentos y Medicamentos de los Estados Unidos) aprobó la goserelina en octubre de 1989.
- Indicación Original: Inicialmente aprobada para el tratamiento del cáncer de próstata.
3. Aprobación por COFEPRIS
[editar]- Fecha de Aprobación: La COFEPRIS (Comisión Federal para la Protección contra Riesgos Sanitarios) en México aprobó la goserelina en 1991.
- Indicación Original: Aprobada para el tratamiento del cáncer de próstata y posteriormente para otras indicaciones como cáncer de mama y endometriosis.
Efectos secundarios
[editar]El acetato de goserelina podría causar un aumento temporal del dolor en los huesos y los síntomas del cáncer de próstata durante las primeras semanas de tratamiento. Esto se conoce como el efecto brote de tumor, y es el resultado de un aumento inicial en la producción de la hormona luteinizante, antes de que los receptores sean desensibilizados y la producción hormonal se inhiba. Los síntomas desaparecerán, con la inhibición hormonal. Por ello es aconsejable co-administrar un antiandrógeno durante las primeras 2-3 semanas de tratamiento con goserelina, particularmente en pacientes con síntomas preexistentes en los huesos. La goserelina podría causar dolor en los huesos, sofocos, cefaleas, dolor abdominal, depresión, dificultad para orinar (casos aislados), aumento de peso, hinchazón y sensibilidad de los senos (poco frecuente), disfunción eréctil y disminución del deseo sexual. El dolor óseo puede ser manejado sintomáticamente, y la disfunción eréctil puede ser tratada con vardenafilo u otras terapias orales similares, a pesar de que no tratarían la disminución del deseo sexual.
Ficha Técnica Detallada de Goserelina (Presentación en México)
[editar]1. Nombre del Medicamento
[editar]- Nombre Genérico: Goserelina
- Nombre Comercial: Zoladex®
2. Composición
[editar]- Ingrediente Activo: Acetato de Goserelina
- Concentración: 3.6 mg y 10.8 mg
3. Forma Farmacéutica
[editar]- Presentación: Implante para administración subcutánea en jeringa prellenada
4. Condiciones de Almacenamiento
[editar]- Conservar en un lugar fresco y seco a temperatura no superior a 25 °C.
- Mantener fuera del alcance de los niños.
5. Presentaciones Comerciales en México
[editar]- Zoladex® 3.6 mg: Caja con una jeringa prellenada con un implante.
- Zoladex® 10.8 mg: Caja con una jeringa prellenada con un implante.
6. Información del Fabricante
[editar]- Laboratorio: AstraZeneca
- Contacto en México: AstraZeneca México, S.A. de C.V.
- Sitio Web: www.astrazeneca.com.mx
7. Fecha de Revisión de la Información
[editar]- Mayo de 2024
- ↑ AstraZeneca official Zoladex site
- ↑ «Copia archivada». Archivado desde el original el 7 de septiembre de 2012. Consultado el 28 de febrero de 2015.
- ↑ FDA Approval for Zoladex 3.6 mg
- ↑ Kotake, Toshihiko; Michiyuki Usami et al. (agosto de 1999). «Goserelin Acetate with or without Antiandrogen or Estrogen in the Treatment of Patients with Advanced Prostate Cancer: a Multicenter, Randomized, Controlled Trial in Japan». Japanese Journal of Clin. Oncol. 29 (11): 562-570. ISSN 1465-3621. PMID 10678560. doi:10.1093/jjco/29.11.562. Consultado el 26 de febrero de 2007.
- ↑ Dittrich R, Binder H, Cupisti S, Hoffmann I, Beckmann MW, Mueller A. Endocrine treatment of male-to-female transsexuals using gonadotropin-releasing hormone agonist. Exp Clin Endocrinol Diabetes 2005;113:586–92.
