Hepatòcit
 | |
| Detalls | |
|---|---|
| Llatí | Hypocrita deforma |
| Part de | fetge |
| Identificadors | |
| MeSH | D022781 |
| TH | H3.04.05.0.00006 |
| FMA | |
| Recursos externs | |
| EB Online | science/hepatocyte |
| Terminologia anatòmica | |
L'hepatòcit és la cèl·lula pròpia del fetge i que forma la seva parènquima, està polaritzada amb dominis luminals diferents i separats dels dominis basals.
Aquestes cèl·lules constitueixen al voltant del 80% del pes de totes les cèl·lules del teixit hepàtic.
L'hepatòcit està situat fisiològicament a la interfície entre l'«exterior» de l'organisme i el medi intern, desenvolupa funcions com: el catabolisme de fàrmacs i tòxics, la formació de bilis, el metabolisme de lípids, la síntesi de proteïnes i el metabolisme d'hidrats de carboni.[1][2][3]
Embriologia
[modifica]Els hepatòcits tenen un origen embriològic comú juntament amb els colangiòcits (cèl·lules epitelials del ducte biliar) a partir de la cèl·lula fundadora anomenada hepatoblast. La separació dels llinatges d'hepatòcits i colangiòcits en humans es produeix a la meitat del segon trimestre de l'embriogènesi.
L'hepatoblast deriva de cèl·lules de l'endoderm multipotencial, ubicades al diverticle hepàtic que és un engrossiment de l'intestí anterior de l'embrió.[4]
Estructura
[modifica]Els hepatòcits constitueixen al voltant del 80% del volum i 60-65% del nombre cel·lular total del teixit hepàtic. Es distribueixen associats a fibres reticulars del teixit connectiu que es projecten des dels espais portals on es distribueixen els vasos sanguinis i els conductes biliars.[5]
Microarquitectura
[modifica]Amb el microscopi òptic els hepatòcits es veuen com a cèl·lules prismàtiques amb un diàmetre de 20-40 μm (en comparació, un pèl humà té un diàmetre 17 a 180 μm).[6] El volum típic d'un hepatòcit és 3.4 x 10−9 cm3.[7]
Presenten el citoplasma acidòfil amb cossos basòfils i són molt rics en orgànuls. A més, contenen inclusions de glucogen i greix al seu citoplasma.[5]
Mostren 2 nuclis esfèrics en 20-25% de les cèl·lules, amb un nuclèol prominent.
La disposició del teixit connectiu i les seves fibres reticulars, que es projecten des dels espais portal, determinen una arquitectura multicel·lular, en zones que són anomenats «petits lòbuls».
-
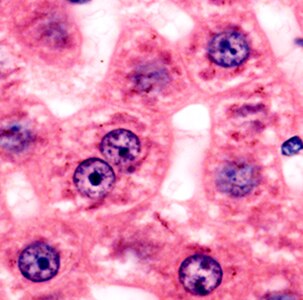
Hepatòcits amb citoplasma en rosat (acidòfil) i nuclis en blau, formant cordons. Microscopi òptic. Tinció d'hematoxilina-eosina
-
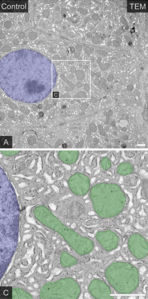
Hepatòcit A) Citoplasma en gris. Nucli pintat en blau. C) Mitocondris en verd. Microscopi electrònic
-
Fibres de reticulina al petit lòbul (color negre) determinant cordons estrets i disposició radial des de l'espai portal (a dalt). Hepatòcits (en verd)
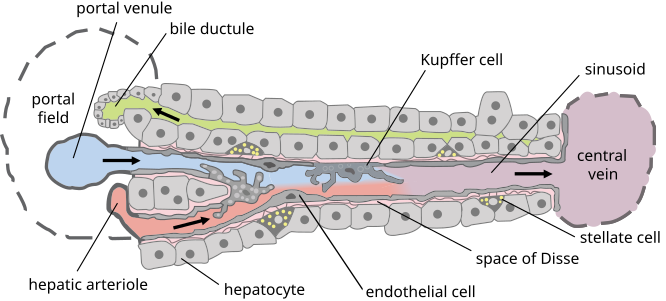
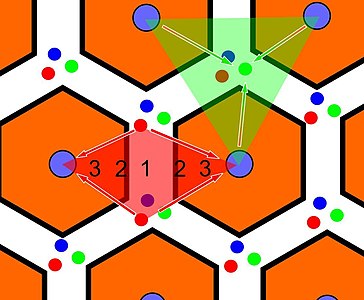
Quan es considera la irrigació arterial dels hepatòcits, aquests es disposen en cordons dins d'un espai amb forma de triangle amb base en dos espais portal i les seves respectives branques interlobul·lars i amb vèrtex allunyat a la vena central lobul·lar. Aquest espai triangular és la menor unitat funcional hepatocítica, va ser anomenada «acinus».[3][5]
-
Unitat elemental de l'acinus: arterioles hepàtica (en vermell), vena porta (en blau), cordó d'hepatòcits, canalicle biliar (en verd), vena central.
Si el que es considera és el drenatge venós, el lòbul hepàtic està format per cordons d'hepatòcits, que es disposen en forma radial, en un espai hexagonal amb centre a la vena centrolobul·lar.[5][8]
-
Acinus en vermell. Petit lòbul en taronja. Espai portal en verd
La bilis produïda pels hepatòcits s'aboca en una xarxa de petits canals dins de les làmines d'hepatòcits i flueix en forma centrífuga cap al lòbul, cap als conductes biliars dels espais porta.
Ultraestructura
[modifica]La membrana plasmàtica dels hepatòcits presenta un domini sinusoide amb microvil·li que miren cap a l'espai de Disse i un domini lateral que mira cap a l'hepatòcit veí, on les membranes dels dos es fusionen per delimitar els petits canals biliars on inicia la via biliar intrahepàtica.
Els mitocondris són nombrosos, fins a 1000 per hepatòcit, ovoides o cilíndrics amb aspecte de bastó, de vegades allargades fins a 2 μm de longitud i es localitzen a prop del nucli i del reticle. Mostren grànuls densos a la seva matriu mitocondrial, formats per calci, ferro i magnesi.[9]
El reticle endoplàsmic és abundant, tant al sector de reticle endoplasmàtic rugós com al sector de reticle endoplasmàtic llis.
-
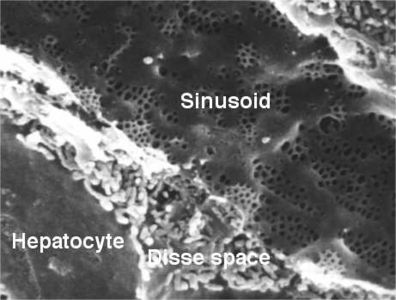
Hepatòcit i sinusoide (vénula) en una secció de fetge de rata
-
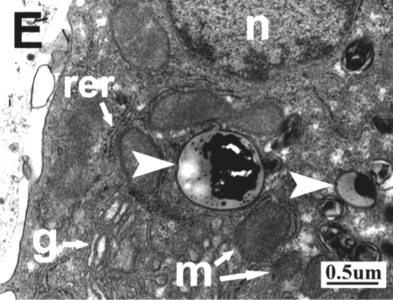
Aparell de Golgi (g), reticle endoplàsmic rugós (rer)
L'aparell de Golgi és gran, és a prop del pol biliar i està format per cinc i més cisternes grans, amb dilatacions saculars i vesícules associades.
-
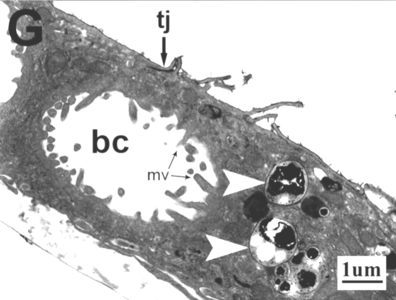
Petits canals biliar (bc) amb microvil·li (mv) de l'hepatòcit al seu interior. Unió estreta (tj) entre dos hepatòcits
-
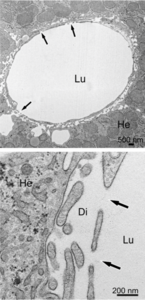
Lumen (Lu), espai de Disse, (Di) hepatòcit (He)
Les vesícules són abundants tant al pol vascular com al biliar.
Els orgànuls a l'hepatòcit es relacionen amb les seves múltiples funcions en el metabolisme de proteïnes, hidrats de carboni, i lípids, i la formació de bilis.
Cada hepatòcit té una organització multipolar; participa en diversos lúmens estrets de petits canals biliars, i té múltiples superfícies basals que s'enfronten al revestiment endotelial de sinusoides.[2]
Funció
[modifica]L'hepatòcit està situat fisiològicament a la interfície entre l'exterior de l'organisme, (representat per la vena porta de sang variable, que arriba des dels intestins, pàncrees, i melsa), i el medi intern arterial constant i filtrat.[10]
Cada hepatòcit compleix centenars de funcions, tant endocrines com exocrines.[11] Algunes són:
- gluconeogènesi,
- síntesi i emmagatzematge de proteïnes; L'hepatòcit és una cèl·lula del cos que fabrica l'albúmina sèrica, el fibrinogen i el grup de factors de coagulació de la protrombina (excepte els factors 3 i 4). És el lloc principal per a la síntesi de lipoproteïnes, ceruloplasmina, transferrina, complement i glicoproteïnes. Els hepatòcits fabriquen les seves pròpies proteïnes estructurals i enzims intracel·lulars. La síntesi de proteïnes es fa mitjançant el reticle endoplasmàtic rugós, i tant el reticle endoplasmàtic rugós com llis estan implicats en la secreció de les proteïnes formades. El reticle endoplasmàtic està implicat en la conjugació de proteïnes amb fragments de lípids i carbohidrats sintetitzats pels hepatòcits o modificats dins dels mateixos. Les proteïnes produïdes pels hepatòcits que funcionen com a hormones es coneixen com a hepatocines.
- metabolisme d'hidrats de carboni (lipogènesi); El fetge forma àcids grassos a partir dels hidrats de carboni i sintetitza triglicèrids a partir d'àcids grassos i glicerol.[12] Els hepatòcits també sintetitzen apoproteïnes amb les quals després s'assemblen i exporten lipoproteïnes (VLDL, HDL). El fetge també és el lloc principal del cos per a la gluconeogènesi, la formació d'hidrats de carboni a partir de precursors com l'alanina, el glicerol i l'oxalacetat.
- formació de bilis,
- catabolisme de fàrmacs i tòxics; Els hepatòcits tenen la capacitat de metabolitzar, desintoxicar i inactivar compostos exògens com els fàrmacs (vegeu metabolisme dels fàrmacs), els insecticides i els compostos endògens com els esteroides. El drenatge de la sang venosa intestinal al fetge requereix una desintoxicació eficient de diverses substàncies absorbides per mantenir l'homeòstasi i protegir el cos de les toxines ingerides. Una de les funcions desintoxicants dels hepatòcits és modificar l'amoníac en urea per a l'excreció. L'orgànul més abundant a les cèl·lules hepàtiques és el reticle endoplasmàtic llis.
- metabolisme de lípids; El fetge rep molts lípids del sistema circulatori i metabolitza les restes de quilomicrons. També sintetitza colesterol a partir d'acetat i sintetitza encara més l'àcid biliar. El fetge és l'únic lloc de formació d'àcid biliar.
Els hepatòcits funcionen en concert amb colangiòcits (cèl·lules epitelials biliars), cèl·lules endotelials, cèl·lules endotelials sinusoïdals, cèl·lules de Kupffer (macròfags hepàtics residents), cèl·lules de fossa (cèl·lules assassines naturals) i cèl·lules estrellades hepàtiques.[13]
Els hepatòcits secreten factor de creixement de l'endoteli vascular (VEGF en anglès), que permet la proliferació i supervivència de les cèl·lules endotelials sinusoïdals, així com la seva capacitat per formar fenestracions.[14]
Recanvi cel·lular d'hepatòcits
[modifica]
El recanvi dels hepatòcits és baix i tenen una vida relativament llarga que s'ha calculat en 120-150 dies.[15]
El fetge és un dels pocs òrgans dels mamífers que mostren canvis a la poliploïdia durant l'homeòstasi, la regeneració i la resposta al dany.[16]
En condicions d'homeòstasi, els hepatòcits ja diferenciats tenen el potencial de regenerar part del parènquima, mitjançant hipertròfia i hiperplàsia compensatòria.[10][17]
En un percentatge variable 20-25% s'observen dos nuclis en un hepatòcit, d'origen endomitòtic per cariocinesi sense citocinesi.[3] És habitual trobar nuclis diploides (16-44%) i tetraploides (55-80%).[5]
Quan el dany hepàtic és extens, es produeix la regeneració intervinguda per cèl·lules mare/progenitores, (LSPC, Liver stem progenitor cell), també anomenades cèl·lules mare/progenitores hepàtiques (HSPC, Hepatic stem progenitor cell), cèl·lules progenitores hepàtiques (LPC, Liver progenitor cell) o cèl·lules progenitores hepàtiques (HPC, Hepatic progenitor cell), que s'ubiquen al petit cabak biliar de Hering, i donen origen a les cèl·lules ovals, que condueixen la regeneració.[4][10][17]
A la lesió hepàtica crònica apareix una reacció ductular a la regió periportal, composta de cèl·lules diferenciades i cèl·lules progenitores hepàtiques (LPC) dins d'una matriu extracel·lular complexa, que conté cèl·lules inflamatòries, cèl·lules endotelials i cèl·lules mesenquimals.[15]
Ús en la investigació
[modifica]Els hepatòcits primaris s'utilitzen habitualment en la investigació biològica i biofarmacèutica cel·lular. Els sistemes de models in vitro basats en hepatòcits han estat de gran ajuda per entendre millor el paper dels hepatòcits en els processos (pato)fisiològics del fetge. A més, la indústria farmacèutica ha confiat molt en l'ús d'hepatòcits en suspensió o cultiu per explorar els mecanismes del metabolisme dels fàrmacs i fins i tot predir el metabolisme dels fàrmacs in vivo.
Amb aquests propòsits, els hepatòcits solen aïllar-se del fetge o del teixit hepàtic sencer animal o humà[18] mitjançant la digestió de col·lagenasa, que és un procés de dos passos. En el primer pas, el fetge es col·loca en una solució isotònica, en la qual s'elimina el calci per trencar les unions estretes cèl·lules-cèl·lules mitjançant l'ús d'un agent quelant del calci. A continuació, s'afegeix una solució que conté colagenasa per separar els hepatòcits de l'estroma hepàtic. Aquest procés crea una suspensió d'hepatòcits, que es poden sembrar en plaques de diversos pous i cultivar-se durant molts dies o fins i tot setmanes. Per obtenir resultats òptims, primer s'han de recobrir les plaques de cultiu amb una matriu extracel·lular (per exemple, col·lagen, Matrigel) per promoure la fixació d'hepatòcits (normalment entre 1 i 3 hores després de la sembra) i el manteniment del fenotip hepàtic. A més, sovint es realitza una superposició amb una capa addicional de matriu extracel·lular per establir un cultiu sandvitx d'hepatòcits. L'aplicació d'una configuració sandvitx admet el manteniment prolongat dels hepatòcits en cultiu.[19] [20]
Els hepatòcits recentment aïllats que no s'utilitzen immediatament es poden criopreservar i emmagatzemar.[21] No proliferen en el cultiu. Els hepatòcits són molt sensibles als danys durant els cicles de criopreservació, incloent la congelació i la descongelació. Fins i tot després de l'addició de crioprotectors clàssics encara hi ha danys mentre es criopreserva.[22] No obstant això, els recents protocols de criopreservació i reanimació donen suport a l'aplicació d'hepatòcits criopreservats per a la majoria d'aplicacions biofarmacèutiques.[23]
Referències
[modifica]- ↑ Repetto, 1997, p. 195.
- ↑ 2,0 2,1 Treyer i Müsch, 2013, p. 243-287.
- ↑ 3,0 3,1 3,2 Welsch i Sobotta, 2009, p. 390-394.
- ↑ 4,0 4,1 Lorenti, 2001, p. 614-620.
- ↑ 5,0 5,1 5,2 5,3 5,4 Kuntz i Kuntz, 2009, p. 25-29.
- ↑ «Diameter of a human hair» (en anglès). The Physics Factbook, 1999. «El diàmetre del cabell humà oscil·la entre 17 a 181 μm.»
- ↑ Lodish et al., Baltimore, p. 10.
- ↑ Moore i Dalley, 2009.
- ↑ Herrerías et al., 1996, p. I,51-I,52.
- ↑ 10,0 10,1 10,2 Tanaka et al., 2011, p. 231-239.
- ↑ Rojas Lemus et al., Cano Gutiérrez.
- ↑ Ali et al., Rychkov, p. 2135-2146.
- ↑ Si-Tayeb, Lemaigre i Duncan, 2010, p. 175-189.
- ↑ Herrnberger et al., Goepferich, p. e115005.
- ↑ 15,0 15,1 Gilgenkrantz i Collin de l'Hortety, 2018.
- ↑ Donne et al., Desdouets.
- ↑ 17,0 17,1 Kholodenko i Yarygin, 2017.
- ↑ Lecluyse i Alexandre, 2010, p. 57-82.
- ↑ Dunn et al., 1989, p. 174-177.
- ↑ De Bruyn et al., Nicolaï, p. 589-616.
- ↑ Li, 2001, p. 357-366.
- ↑ Hamel et al., Sarhan, p. 661-670.
- ↑ De Bruyn et al., Baes, p. 297-307.
Bibliografia
[modifica]- Ali, E. S.; Hua, J.; Wilson, C. H.; Tallis, G. A.; Zhou, F. H.; Rychkov, G. Y.; Barritt, G. J. «The glucagon-like peptide-1 analogue exendin-4 reverses impaired intracellular Ca2+ signalling in steatotic hepatocytes» (en anglès). Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, 1863(9), 2016. DOI: 10.1016/j.bbamcr.2016.05.006. PMID: 27178543.
- De Bruyn, T.; Ye, Z. W.; Peeters, A.; Sahi, J.; Baes, M.; Augustijns, P. F.; Annaert, P. P. «Determination of OATP-, NTCP- and OCT-mediated substrate uptake activities in individual and pooled batches of cryopreserved human hepatocytes» (en anglès). Eur. J. Pharm. Sci., 43(4), juliol 2011. DOI: 10.1016/j.ejps.2011.05.002. PMID: 21605667.
- De Bruyn, T.; Chatterjee, S.; Fattah, S; Keemink, J.; Nicolaï, J; Augustijns, P.; Annaert, P. «Sandwich-cultured hepatocytes: utility for in vitro exploration of hepatobiliary drug disposition and drug-induced hepatotoxicity» (en anglès). Expert Opin Drug Metab Toxicol, 9(5), maig 2013. DOI: 10.1517/17425255.2013.773973. PMID: 23452081.
- Donne, R.; Saroul-Aïnama, M.; Cordier, P.; Celton-Morizur, S.; Desdouets, C. «Polyploidy in Liver Development, Homeostasis and Disease» (en anglès). Nat. Rev. Gastroenterol Hepatol., 2020.
- Dunn, J. C.; Yarmush, M. L.; Koebe, H. G.; Tompkins, R. G. «Hepatocyte function and extracellular matrix geometry: long-term culture in a sandwich configuration» (en anglès). FASEB J., 3(2), febrer 1989. DOI: 10.1096/fasebj.3.2.2914628. PMID: 2914628. Erratum en: FASEB J 1989 Maig; 3(7):1873.
- Gilgenkrantz, H.; Collin de l'Hortety, A. (en anglès) The American Journal of Pathology, 188(6), 2018.
- Hamel, F.; Grondin, M. L.; Denizeau, F.; Averill-Bates, D. A.; Sarhan, F. «Wheat extracts as an efficient cryoprotective agent for primary cultures of rat hepatocytes» (en anglès). Biotechnology and Bioengineering, 95(4), 2006. DOI: 10.1002/bit.20953. PMID: 16927246.
- Herrerías, P.; Ramón, G.; Cabrera, L.; Lira, J. «Cap. 4: Ultraestructura normal y patología del hígado». A: Tratado de Hepatología (en castellà). Universitat de Sevilla, 1996.
- Herrnberger, L.; Hennig, R.; Kremer, W.; Hellerbrand, C.; Goepferich, A.; Kalbitzer, H. R. «Formation of Fenestrae in Murine Liver Sinusoids Depends on Plasmalemma Vesicle-Associated Protein and Is Required for Lipoprotein Passage» (en anglès). PLoS ONE, 9(12), 2014.
- Kholodenko, I. V.; Yarygin, K. N. «Cellular Mechanisms of Liver Regeneration and Cell-Based Therapies of Liver Diseases» (en anglès). BioMed Research International, 2017(8910821), 2017.
- Kuntz, E.; Kuntz, H. D.. «Cap. 3: Morphology of the Liver». A: Hepatology: Textbook and Atlas (en anglès). Springer Science & Business Media, 2009.
- Lecluyse, E. L.; Alexandre, E. «Isolation and culture of primary hepatocytes from resected human liver tissue». A: Hepatocytes (en anglès). 640, 2010 (Methods Mol. Biol.). DOI 10.1007/978-1-60761-688-7_3. ISBN 978-1-60761-687-0.
- Li, Albert P. «Screening for human ADME/Tox drug properties in Drug Discovery» (en anglès). Drug Discovery Today, 6(7), 2001. DOI: 10.1016/s1359-6446(01)01712-3. PMID: 11267922.
- Lodish, H.; Berk, A.; Zipursky, S. L.; Matsudaira, P.; Baltimore, D.; Darnell, J. E. Molecular Cell Biology (en anglès). Nova York: W. H. Freeman and Company, 2000.
- Lorenti, A. S. «Células Progenitoras Hepáticas» (en anglès). Medicina [Buenos Aires], 61(5.1), 2001.
- Moore, Keith L.; Dalley, Arthur F. Anatomía con orientación clínica (en castellà). Médica Panamericana, 2009. ISBN 9789687988894.
- Repetto, Manuel. «Hepatopatía tóxica». A: Toxicología Fundamental (en castellà). Ediciones Díaz de Santos, 1997. ISBN 9788479782634.
- Rojas Lemus, M.; Milán Chávez, R.; Delgado Medina, A.; Bizarro Nevares, P.; Cano Gutiérrez, G.; Cafaggi Padilla, D.; Cervantes Yépez, S.; Fortoul van der Goes, T. I. «El hepatocito como un ejemplo de interacción entre la biología celular y las rutas metabólicas» (en castellà). Rev. Fac. Med. [Ciutat de Mèxic], 60(2), 2017.
- Si-Tayeb, K.; Lemaigre, F. P.; Duncan, S. A. «Organogenesis and Development of the Liver» (en anglès). Cell, 18(2), 2010.
- Tanaka, M.; Itoh, T.; Tanimizu, N.; Miyajima, A. «Liver stem/progenitor cells: their characteristics and regulatory mechanisms» (en anglès). The Journal of Biochemistry, 149(3), 2011.
- Treyer, A.; Müsch, A. «Hepatocyte Polarity» (en anglès). Compr. Physiol., 3(1), 2013. DOI: 10.1002/cphy.c120009.
- Welsch, U.; Sobotta, J. «Cap. 10: Aparato Digestivo». A: Histología (en castellà). Médica Panamericana, 2009.
Vegeu també
[modifica]Enllaços externs
[modifica]- «La histologia hepàtica: Hepatòcits» (en anglès). Colorado State University. Arxivat de l'original el 2023-05-29. [Consulta: 11 febrer 2011].