Histona H2B
La histona H2B es una de las cinco familias principales de proteínas histonas involucradas en el mantenimiento de la estructura de los nucleosomas y de la cromatina en células eucariotas. Contienen un dominio globular principal y extremos largos N- y C-terminal.[1]
Las otras familias de histonas son: H1, H2A, H3 y H4.
Estructura
[editar]
La histona H2B es una proteína estructural pequeña, compuesta de 126 aminoácidos.[2] Muchos de estos aminoácidos tienen carga positiva a pH celular, lo cual le permite interaccionar con los grupos fosfato del ADN, que tiene carga negativa.[3] Además de un dominio globular central, H2B tiene 2 colas N- y C-terminal flexibles que se extienden hacia fuera. Estas participan en la condensación de la cromatina a partir de la conformación de fibras de 30 nanómetros (nm) en forma de "collar de cuentas".[3] Al igual que otras histonas, H2B tiene un plegamiento único y optimizado para interacciones histona-histona e histona-ADN.[1]
Dos copias de H2B se unen con otras dos de cada histona H2A, H3 y H4 para formar un octámero en el centro del nucleosoma[2] y empaquetar el ADN.[3] Para facilitar esta formación, H2B se une primero a H2A para formar un heterodímero.[2] Dos de estos heterodímeros se unen con un heterotetrámero de H3 y H4, dando al nucleosoma su característica forma en disco.[3] El ADN se enrolla alrededor del nucleosoma en grupos de aproximadamente 160 nucleótidos.[1] El enrollamiento continua hasta que toda la cromatina ha sido empaquetada con los nucleosomas.[4]
Función
[editar]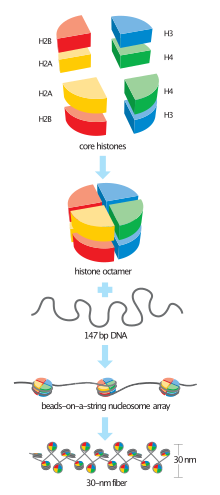
La histona H2B es una proteína estructural que participa en la organización del ADN eucariótico.[5] Desempeña un papel importante en la biología del núcleo celular, donde participa en el empaquetamiento y mantenimiento de los cromosomas,[5] la regulación de la transcripción, la replicación y la reparación del ADN.[2] También colabora en la regulación de la estructura y función de la cromatina a través de modificaciones postraduccionales y variantes de histonas especializadas.[4]
La acetilación y la ubiquitinación son ejemplos de dos tipos de modificaciones postraduccionales que afectan a la función de la histona H2B de manera particular. La hiperacetilación de las colas de las histonas ayuda a las proteínas de unión al ADN a acceder a la cromatina al debilitar las interacciones histona-ADN y nucleosoma-nucleosoma.[6] Además, la acetilación de un residuo de lisina específico promueve la unió a los bromodominios de ciertas proteínas reguladoras de la transcripción. Este acoplamiento facilita el reclutamiento de estas proteínas en la región correcta del cromosoma. La histona H2B ubiquitinizada se encuentra a menudo en regiones de transcripción activa.[6] Al favorecer la remodelación de la cromatina, H2B estimula la elongación transcripcional y prepara el escenario para modificaciones adicionales que regulan múltiples elementos de la transcripción.[6] En concreto, la ubiquitina en la histona H2B abre y despliega regiones de cromatina, permitiendo el acceso de la maquinaria de transcripción a las regiones promotoras del ADN.[7]
Si bien solo se han estudiado en profundidad unas pocas isoformas de la histona H2B, se ha comprobado que sus variantes cumplen funciones relevantes. Si ciertas variantes dejaran de funcionar, los centrómeros no se formarían correctamente, se perdería la integridad del genoma y se silenciaría la respuesta al daño del ADN.[4] En determinados organismos eucariotas inferiores, una variante de histona H2B se une a una variante de histona H2A llamada H2AZ, se localiza en genes activos y promueve la transcripción en esas regiones. En ratones, la variante H2BE ayuda a controlar la expresión de genes relacionados con el olfato. Esto apoya la idea de que las isoformas de la histona H2B pueden tener funciones especializadas en diferentes tejidos.[4]
Isoformas
[editar]Se han identificado 16 variantes de la histona H2B en humanos, de las cuales 13 se expresan en cuerpos celulares y 3 solo se expresan en testículos. Estas variantes, también llamadas isoformas, son proteínas que son estructuralmente muy similares a la histona canónica H2B, aunque presentan algunas variaciones específicas en su secuencia de aminoácidos.[4] Todas las variantes de H2B contienen el mismo número de aminoácidos, y tienen pocas variaciones en la secuencia. Solo dos de los cinco aminoácidos cambian, pero incluso estas pequeñas diferencias pueden cambiar la estructura de las isoformas.[4]
Las isoformas de H2B interactúan de manera diferente con otras proteínas, se encuentran en regiones específicas de la cromatina, tienen diferentes tipos y número de modificaciones postraduccionales y son más o menos estables que la histona canónica H2B. Todas estas diferencias causan que las isoformas tengan funciones únicas, incluso funciones diferentes en función del tejido.[4]
Muchas isoformas de H2B se expresan de manera independiente de la replicación del ADN. Se producen al mismo nivel a lo largo de las fases del ciclo celular. La histona canónica H2B solo se añade a los nucleosomas durante la fase S del ciclo celular cuando se produce la replicación del ADN. Las isoformas se añaden en otras fases. Se puede consultar información de estas isoformas en la base de datos HistoneDB with Variants.
Modificaciones postraduccionales
[editar]La histona H2B se modifica por una combinación de diferentes modificaciones postraduccionales.[1] Estas modificaciones afectan a la estructura y función de la histona en la organización de la cromatina,[8] y la mayoría de estas se encuentran en el exterior del dominio globular del nucleosoma, donde los aminoácidos son más accesibles.[7] Entre las modificaciones se incluyen: acetilación, metilación, fosforilación, ubiquitinización y sumoilación.[8] La acetilación, fosforilación y ubiquitinización son las más comunes y mejor estudiadas.
Acetilación
[editar]H2B se encuentra tanto en promotores como en regiones codificantes de genes, donde existen patrones específicos de hiperacetilación e hipoacetilación en determinados residuos de lisina en la cola N-terminal.[8] La acetilación depende de histonas acetilatransferasas específicas que trabajan en promotores de genes durante la activación transcripcional.[1] La adición de un grupo acetilo a las lisinas en los extremos de H2B contribuye a la activación de la transcripción.[3] La comunidad científica considera que la acetilación de la cola N-terminal, por ejemplo en H2BK5ac, cumple una parte importante en la regulación transcripcional.[8]
O-GlcNAcilación
[editar]Se cree que la modificación de H2B S112 con un grupo O-β-N-acetilglucosamina facilita la monoubiquitinización de K112, lo cual está asociado con regiones transcripcionalmente activas.[9]
Fosforilación
[editar]En H2B la fosforilación de serinas o treoninas activa la transcripción.[3] Cuando ocurre estrés metabólico en la célula, una kinasa activada por AMP fosforila la lisina en posición 36 de la histona H2B del promotor y regiones codificantes del ADN, lo cual ayuda a la regulación de la elongación transcripcional.[2] Si la célula recibe múltiples estímulos de apoptosis, la caspasa-3 activa a la kinasa Mst1, la cual fosforila la serina en posición 14 de todas las histonas H2B, lo cual facilita la condensación de la cromatina. Los daños en el ADN pueden inducir la misma respuesta a una escala más local y de manera rápida para facilitar la su reparación.[2]
Ubiquitinización
[editar]Los residuos de ubiquitina se suelen añadir a la lisina en posición 120 de la histona H2B, lo cual activa la transcripción.[3] Se han identificado otros sitios de ubiquitinización en los últimos años, aunque no están tan bien estudiadas.[4] Las enzimas de conjugación de ubiquitina y ligasas de ubiquitina regulan la ubiquitinización de H2B. Estas enzimas se cotranscriben para conjugar la ubiqituina en H2B. Los niveles de ubiqutinización pueden variar a lo largo del ciclo celular, siendo retiradas en la metafase y reconjugadas en la anafase.[7]
Genética
[editar]La secuencia de aminoácidos de H2B está altamente conservada evolutivamente. Incluso especies distantes en la evolución tienen histonas H2B extremadamente similares.[3] La familia H2B contiene 214 miembros de diferentes especies. En humanos H2B está codificada por 23 genes diferentes,[10] ninguno de los cuales contienen intrones.[2] Todos estos genes se localizan en el clúster de histonas 1 en el cromosoma 6 y los clústers 2 y 3 en el cromosoma 1. En cada clúster de genes, los genes que codifican para H2B comparten una región promotora con secuencias que codifican para la histona H2A. Mientras que todos los genes del clúster de histonas se transcriben en altos niveles durante la fase S, los genes individuales de H2B también se expresan en otros momentos durante el ciclo celular. Están dualmente reguladas tanto por los promotores del clúster como por sus promotores específicos.[4]
Véase también
[editar]- Código de histonas
- Nucleosoma
- Cromatina
- Otras proteínas histonas:
Referencias
[editar]- ↑ a b c d e Reche, Pedro A.; Keskin, Derin B.; Hussey, Rebecca E.; Ancuta, Petronela; Gabuzda, Dana; Reinherz, Ellis L. (18 de mayo de 2006). «Recognition and classification of histones using support vector machine». Journal of Computational Biology 13 (1): 102-12. PMID 16472024. doi:10.1186/1476-9433-5-1. Consultado el 9 de octubre de 2022.
- ↑ a b c d e f g Rønningen, Torunn; Shah, Akshay; Oldenburg, Anja R.; Vekterud, Kristin; Delbarre, Erwan; Moskaug, Jan Øivind; Collas, Phillippe (December 2015). «Prepatterning of differentiation-driven nuclear lamin A/C-associated chromatin domains by GlcNAcylated histone H2B». Genome Research 25 (12): 1825-35. PMC 4665004. PMID 26359231. doi:10.1101/gr.193748.115. Consultado el 9 de octubre de 2022.
- ↑ a b c d e f g h Lodish, Harvey F. (1 de agosto de 2012). Molecular Cell Biology (Seventh edición). New York: W. H. Freeman & Company. pp. 258-328. ISBN 978-1-4292-3413-9.
- ↑ a b c d e f g h i Molden, Rosalynn C.; Bhanu, Natarajan V.; LeRoy, Gary; Arnaudo, Anna M.; Garcia, Benjamin A. (22 de abril de 2015). «Multi-faceted quantitative proteomics analysis of histone H2B isoforms and their modifications». Epigenetics & Chromatin 8 (15): 15. PMC 4411797. PMID 25922622. doi:10.1186/s13072-015-0006-8. Consultado el 9 de octubre de 2022.
- ↑ a b Wu, Jiangli; Mu, Shumei; Guo, Mingshen; Chen, Tingrong; Zhang, Zhaohui; Li, Zhenqiu; Li, Yanqin; Kang, Xianjiang (Enero de 2016). «Histone H2B gene cloning, with implication for its function during nuclear shaping in the Chinese mitten crab, Eriocheir sinensis». Gene 575 (2 Pt 1): 276-84. PMID 26343795. doi:10.1016/j.gene.2015.09.005. Consultado el 9 de octubre de 2022.
- ↑ a b c «Histone H2B (53H3) Mouse mAb #2934». Cell Signaling Technology. Consultado el 24 de noviembre de 2015.
- ↑ a b c Osley, Mary Ann (Septiembre de 2006). «Regulation of histone H2A and H2B ubiquitylation». Briefings in Functional Genomics & Proteomics 5 (3): 179-89. PMID 16772277. doi:10.1093/bfgp/ell022. Consultado el 9 de octubre de 2022.
- ↑ a b c d Golebiowski, Filip; Kasprzak, Kazimierz S. (Noviembre de 2005). «Inhibition of core histones acetylation by carcinogenic nickel(II)». Molecular and Cellular Biochemistry 279 (1–2): 133-9. PMID 16283522. doi:10.1007/s11010-005-8285-1. Consultado el 9 de octubre de 2022.
- ↑ Fujiki, R.; Chikanishi, Toshihiro; Hashiba, Waka; Ito, Hiroaki; Takada, Ichiro; S, Roeder; Robert, G.; Kitagawa, Hirochika et al. (27 de noviembre de 2011). «GlcNAcylation of Histone H2B Facilitates Its Monoubiquitination». Nature (en inglés) 480 (7378): 557-60. Bibcode:2011Natur.480..557F. PMC 7289526. PMID 22121020. doi:10.1038/nature10656. Consultado el 9 de octubre de 2022.
- ↑ «Histone H2B». HIstome: A Relational Knowledgebase of Human Proteins and Histone Modifying Enzymes. Nucleic Acids Research. Archivado desde el original el 16 de octubre de 2016. Consultado el 24 de noviembre de 2015.
