Lithiumnitride
| Lithiumnitride | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
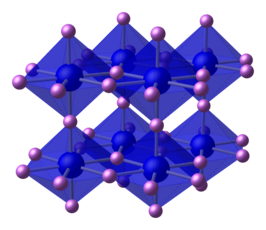
| ||||
Eenheidscel van , ball and stick model
| ||||
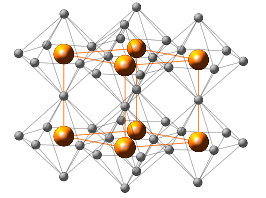
| ||||
Kristalstructuur van
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| Andere namen | Trilithiumnitride | |||
| Molmassa | 34,83 g/mol | |||
| SMILES | [Li]N([Li])[Li]
| |||
| CAS-nummer | 26134-62-3 | |||
| EG-nummer | 247-475-2 | |||
| PubChem | 520242 | |||
| Wikidata | Q413407 | |||
| Beschrijving | rood-purperen vaste stof | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H260 - H314 | |||
| P-zinnen | P223 - P231+P232 - P260 - P264 - P280 - P301+P330+P331 - P303+P361+P353 - P304+P340 - P305+P351+P338 - P310 - P321 - P335+P334 - P363 - P370+P378 - P402+P404 - P405 - P501 | |||
| Fysische eigenschappen | ||||
| Dichtheid | 1,270 g/cm³ | |||
| Smeltpunt | 813 °C | |||
| Oplosbaarheid in water | reageert g/L | |||
| log(Pow) | 3,24 | |||
| Thermodynamische eigenschappen | ||||
| ΔfG |
[1] -207 kJ/mol | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Lithiumnitride is een chemische verbinding met de formule . Het is het enige stabiele alkali-nitride. De vaste stof heeft een rood-roze kleur en een hoog smeltpunt.[2] Naast zijn ook bij hogere drukken en bekend.[1][3]
Synthese en risico
[bewerken | brontekst bewerken]Lithiumnitride wordt verkregen door de directe reactie tussen lithium en stikstofgas.[4]
In plaats van metallisch lithium in een stikstofatmosfeer te verbanden wordt een oplossing van lithium in vloeibaar natrium met stikstofgas behandeld. Deze reactie verloopt al bij kamertemperatuur, maar dan erg langzaam. De reactie wordt meestal uitgevoerd bij ongeveer 100, een temperatuur net boven de smelttemperatuur van natrium.[1]
Lithiumnitride reageert heftig met water, waarbij ammoniak ontstaat:
Wordt lithiumnitride in een waterstofstroom verhit, dan ontstaat via lithiumamide en lithiumimide uiteindelijk lithiumhydride en stikstofgas:[1][5][6]
Structuur en eigenschappen
[bewerken | brontekst bewerken](stabiel onder standaardomstandigheden) heeft een ongebruikelijke kristalstructuur: het bestaat uit twee soorten lagen. De ene heeft de samenstelling , de stukstof-atomen zijn hierin 6 gecoördineerd, de andere laag bestaat uitsluitend uit lithium-kationen.[7]
Naast de alfa-vorm zijn ook en bekend. De beta-vorm ontstaat uit de alfa-vorm bij 4200 bar = 4,2∙108 Pa met dezelfde kristalstructuur als natriumarsenide. ontstaat uit de beta-vorm bij een druk van ongeveer 4∙1010 Pa en heeft dezelfde kristalstructuur als .[8]
Lithiumnitride is een goede ionengeleider (ladingtransport via ionen in plaats an elektronen).[1][9]
Toepassingen[1]
[bewerken | brontekst bewerken]In de metallurgie wordt lithiumniride toegepast om stikstof aan legeringen toe te voegen.[10]
Lithiumnitride wordt in combinatie met brandstofcellen ook onderzocht als opslagmedium voor waterstof, omdat het door reactie tot 9,3 gewichts% waterstof kan opnemen. De reactie verloopt via lithiumimide en lithiumamide. Omdat de reactie tussen het imide en het amide reversibel is, komt het practische waterstofgehalte uit op 7%. Voor een practische toepassing is momenteel (2023) de werktemperatuur van ongeveer 255 °C te hoog.[11][12][13]
- Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Lithium nitride op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ a b c d e f Toegevoegd vanuit de Duitse Wikipedia naar de tekst van 18 juni 2023. Gearchiveerd op 12 april 2024.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8
- ↑ Dominique Laniel, Gunnar Weck, Paul Loubeyre: Direct Reaction of Nitrogen and Lithium up to 75 GPa: Synthesis of the Li3N, LiN, LiN2, and LiN5 Compounds. In: Inorganic Chemistry. 57, 2018, S. 10685, DOI:10.1021/acs.inorgchem.8b01325.
- ↑ E. Döneges "Lithium Nitride" in Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, New York. Vol. 1. p. 984.
- ↑ R. Abegg, F. Auerbach, I. Koppel: Handbuch der anorganischen Chemie. 2. Band, 1. Teil, Verlag S. Hirzel, 1908, S. 134 (Volltext).
- ↑ K. A. Hofmann: Lehrbuch der anorganischen Chemie. 2. Auflage, Verlag F. Vieweg & Sohn, 1919, S. 441 (Volltext).
- ↑ Barker M. G., Blake A. J., Edwards P. P. (1999). Novel layered lithium nitridonickelates; effect of Li vacancy concentration on N co-ordination geometry and Ni oxidation state. Chemical Communications (13): 1187–1188. DOI: 10.1039/a902962a.
- ↑ Solid-State Hydrogen Storage: Materials and Chemistry (2008).
- ↑ Albrecht Rabenau. (1981). Lithiumnitrid und verwandte Stoffe, Ihre wissenschaftliche und praktische Bedeutung. Sila-Substitutionen pag.: 12 Westdeutscher Verlag GmbH (Opladen) ISBN 978-3-663-01758-5 Google: bibliotheek
- ↑ D. L. Perry, S. L. Phillips: Handbook of Inorganic Compounds: An Electronic Database. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 228.
- ↑ Jan Oliver Löfken. (2019-09-08). Neuer Wasserstoffspeicher aus Lithiumnitrid entdeckt Bild der Wissenschaft. . Gearchiveerd op 18 juni 2023.
- ↑ . (2002-11-25). Neues Speichermedium für Wasserstoff entwickelt innovations-report.de.
- ↑ Ping Chen, Zhitao Xiong, Jizhong Luo, Jianyi Lin, Kuang Lee Tan. (2002). Interaction of hydrogen with metal nitrides and imides Nature. 420 (6913): pag.: 302–304 DOI:10.1038/nature01210
















