സൾഫർ ഡയോക്സൈഡ്

| |
| |
| |
| Names | |
|---|---|
| IUPAC name
Sulfur dioxide
| |
Other names
| |
| Identifiers | |
3D model (JSmol)
|
|
| Beilstein Reference | 3535237 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.028.359 |
| EC Number |
|
| E number | E220 (preservatives) |
| Gmelin Reference | 1443 |
| KEGG | |
| MeSH | {{{value}}} |
PubChem CID
|
|
| RTECS number |
|
| UNII | |
| UN number | 1079, 2037 |
CompTox Dashboard (EPA)
|
|
| InChI | |
| SMILES | |
| Properties | |
| തന്മാത്രാ വാക്യം | |
| Molar mass | 0 g mol−1 |
| Appearance | Colorless and pungent gas |
| Odor | Pungent; similar to a just-struck match[1] |
| സാന്ദ്രത | 2.619 kg m−3[2] |
| ദ്രവണാങ്കം | |
| ക്വഥനാങ്കം | |
| 94 g/L[3] forms sulfurous acid | |
| ബാഷ്പമർദ്ദം | 230 kPa at 10 °C; 330 kPa at 20 °C; 462 kPa at 30 °C; 630 kPa at 40 °C[4] |
| അമ്ലത്വം (pKa) | ~1.81 |
| Basicity (pKb) | ~12.19 |
| −18.2·10−6 cm3/mol | |
| വിസ്കോസിറ്റി | 12.82 μPa·s[5] |
| Structure | |
| C2v | |
| Digonal | |
| Dihedral | |
| 1.62 D | |
| Thermochemistry | |
| Std enthalpy of formation ΔfH |
−296.81 kJ mol−1 |
| Standard molar entropy S |
248.223 J K−1 mol−1 |
| Hazards | |
| GHS pictograms |  
|
| GHS Signal word | Danger |
| H314, H331[6] | |
| Lethal dose or concentration (LD, LC): | |
LC50 (median concentration)
|
3000 ppm (mouse, 30 min) 2520 ppm (rat, 1 hr)[8] |
LCLo (lowest published)
|
993 ppm (rat, 20 min) 611 ppm (rat, 5 hr) 764 ppm (mouse, 20 min) 1000 ppm (human, 10 min) 3000 ppm (human, 5 min)[8] |
| NIOSH (US health exposure limits): | |
PEL (Permissible)
|
TWA 5 ppm (13 mg/m3)[7] |
REL (Recommended)
|
TWA 2 ppm (5 mg/m3) ST 5 ppm (13 mg/m3)[7] |
IDLH (Immediate danger)
|
100 ppm[7] |
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
| |
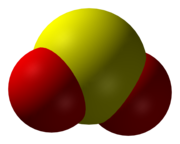
ഒരു സൾഫർ അണുവും രണ്ടു് ഓക്സിജൻ അണുക്കളും അടങ്ങുന്ന തന്മാത്രയുള്ള ഒരു വാതകമാണു് സൾഫർ ഡയോക്സൈഡ്. ഇതിന്റെ രാസവാക്യം SO2 എന്നാണു്. രൂക്ഷമായ തുളച്ചുകയറുന്ന മണമുള്ള ഒരു വാതകമാണിത്. അഗ്നിപർവതങ്ങളിൽ നിന്നും പലതരം വ്യവസായങ്ങളിൽ നിന്നും ഈ വാതകം പുറത്തുവിടാറുണ്ട്. കൽക്കരി പെട്രോളിയം എന്നിവയിൽ സൾഫർ സംയുക്തങ്ങൾ ഉള്ളതുകാരണം ഇവ ജ്വലിക്കുമ്പോൾ സൾഫർ ഡയോക്സൈഡ് ഉണ്ടാകും. SO2, സാധാരണഗതിയിൽ NO2 പോലെയുള്ള രാസത്വരകത്തിന്റെ സാന്നിദ്ധ്യത്തിൽ ഓക്സിഡേഷനു വിധേയമാകുമ്പോൾ H2SO4 ഉണ്ടാകും. ഇത് ആസിഡ് മഴയ്ക്ക് കാരണമാകും.[9] അന്തരീക്ഷത്തിൽ തങ്ങിനിൽക്കുന്ന ധൂളികളും ഇത്തരത്തിൽ ഉണ്ടാകും. ഈ രണ്ടു വിധത്തിലാണ് സൾഫർ ഡയോക്സൈഡ് പ്രധാനമായും പരിസ്ഥിതിയെ ബാധിക്കുന്നത്.
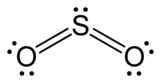
ഘടനയും ബോണ്ടുകളും
[തിരുത്തുക]SO2 ഒരു ഒടിവുള്ള തന്മാത്രയാണ്.

ഉത്പാദനം
[തിരുത്തുക]ജ്വലനത്തിലൂടെ
[തിരുത്തുക]സൾഫറോ സൾഫർ അടങ്ങിയിട്ടുള്ള വസ്തുക്കളോ കത്തിക്കുമ്പോൾ സൾഫർ ഡയോക്സൈഡ് ഉണ്ടാകും:
- S8 + 8 O2 → 8 SO2
കമ്പിളി, മുടി, റബ്ബർ എന്നിവയൊക്കെ കത്തിക്കുമ്പോൾ സൾഫർ ഉണ്ടാകും. ഇരുമ്പുമായി ചേർന്ന് (വീടിനു തീ പിടിക്കുമ്പോഴും മറ്റും) ഇത് ഫെറസ് സൾഫൈഡ് ഉണ്ടാക്കും. ഇതിനെ വീണ്ടും ഓക്സിജന്റെ സാന്നിദ്ധ്യത്തിൽ ചൂടാക്കിയാൽ സൾഫർ ഡയോക്സൈഡ് വീണ്ടും സ്വതന്ത്രമാകും:
4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
ഹൈഡ്രജൻ സൾഫൈഡ് ജ്വലിച്ചാലും രാസപ്രവർത്തനം ഇതുപോലെ തന്നെയാണ് നടക്കുന്നത്.
- 2 H2S + 3 O2 → 2 H2O + 2 SO2
പൈറൈറ്റ്, സ്ഫാലെറൈറ്റ്, സിന്നബാർ തുടങ്ങിയ അയിരുകൾ വ്യാവസായികമായി റോസ്റ്റ് ചെയ്യുമ്പോഴും സൾഫർ ഡയോക്സൈഡ് ഉത്പാദിപ്പിക്കപ്പെടും:[10]
- 4 FeS2 + 11 O2 → 2 Fe2O3 + 8 SO2
- 2 ZnS + 3 O2 → 2 ZnO + 2 SO2
- HgS + O2 → Hg + SO2
- 4 FeS + 7O2 → 2 Fe2O3 + 4 SO2
ഈ രീതികളെല്ലാം ചേർന്നാണ് അഗ്നിപർവതങ്ങളിൽ നിന്ന് ദശലക്ഷക്കണക്കിന് ടൺ സൾഫർ ഡയോക്സൈഡ് പുറത്തുവരുന്നത്.
പ്രതിപ്രവർത്തനങ്ങൾ
[തിരുത്തുക]വ്യാവസായികം
[തിരുത്തുക]ക്ഷാരഗുണമുള്ള ലായനികൾ സൾഫൈറ്റ് ലവണങ്ങളുമായി പ്രതിപ്രവർത്തിക്കുമ്പോൾ:
- SO2 + 2 NaOH → Na2SO3 + H2O
ക്ലൗസ് പ്രക്രീയയിൽ സൾഫർ ഡയോക്സൈഡ് ഒക്സിഡൈസിംഗ് രാസവസ്തുവായാണ് പ്രവർത്തിക്കുന്നത്. റിഫൈനറികളിൽ ഈ രാസപ്രവർത്തനം വൻ തോതിൽ ഉപയോഗിക്കാറുണ്ട്:
- SO2 + 2 H2S → 3 S + 2 H2O
സൾഫ്യൂറിക് ആസിഡിന്റെ നിർമ്മാണം.
- 2 SO2 + 2 H2O + O2 → 2 H2SO4
ഉപയോഗങ്ങൾ
[തിരുത്തുക]സൾഫ്യൂറിക് ആസിഡിന്റെ നിർമ്മാണത്തിലെ ഉപയോഗം
[തിരുത്തുക]ഭക്ഷ്യവസ്തുക്കൾ സൂക്ഷിച്ചുവയ്ക്കാൻ
[തിരുത്തുക]ഉണക്കിയ ആപ്രിക്കോട്ട്, ഫിഗ് തുടങ്ങിയ പഴങ്ങൾ സൂക്ഷിച്ചുവയ്ക്കാൻ സൾഫർ ഡയോക്സൈഡിന്റെ രോഗാണുക്കളെ നശിപ്പിക്കാനുള്ള ശേഷി ഉപയോഗപ്പെടുത്താറുണ്ട്. ചീയൽ തടയുകയും നിറം സംരക്ഷിക്കുകയും ചെയ്യും എന്ന ഗുണവുമുണ്ട്. മൊളാസസ്സിലും ചിലപ്പോൾ ഇത് ചേർക്കാറുണ്ട്.
വൈൻ നിർമ്മാണം
[തിരുത്തുക]വൈനുത്പാദനത്തിൽ സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിക്കാറുണ്ട്.[11] എല്ലാത്തരം വൈനുകളിലും സൾഫർ ഉണ്ടാകും.[12] രോഗാണു നാശിനിയായും ഓക്സിഡേഷൻ തടയുന്ന രാസവസ്തുവായുമാണ് ഇത് പ്രവർത്തിക്കുന്നത്.
SO2 വൈൻ നിർമ്മാണശാലകൾ വൃത്തിയാക്കാനും ഉപയോഗിക്കപ്പെടുന്നുണ്ട്.
റെഡ്യൂസിംഗ് രാസവസ്തുവായുള്ള ഉപയോഗം
[തിരുത്തുക]പേപ്പറിനെ ബ്ലീച്ച് ചെയ്യാൻ ഇതുപയോഗിക്കാറുണ്ട്. ക്ലോറിനേറ്റ് ചെയ്ത ജലത്തെ ഉപയോഗശേഷം ഒഴുക്കിക്കളയുന്നതിനു മുൻപ് സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിച്ച് റെഡ്യൂസ് ചെയ്യാറുണ്ട്. ഇത് ക്ലോറിനെ സ്വതന്ത്രമാക്കും. [13]
ഇത് ജലത്തിൽ ലയിക്കും.
ബയോകെമിസ്ട്രിയിലും വൈദ്യത്തിലുമുള്ള ഉപയോഗം
[തിരുത്തുക]വലിയ അളവിൽ സൾഫർ ഡയോക്സൈഡ് മാരകമാണ്. ബാക്ടീരിയകളും മറ്റും ഇത് ഉത്പാദിപ്പിക്കാറുണ്ട്. സസ്തനികളുടെ ശരീരപ്രവർത്തനത്തിൽ സൾഫർ ഡയോക്സൈഡിന്റെ പ്രഭാവം ഇതുവരെ പൂർണമായി മനസ്സിലാക്കാൻ സാധിച്ചിട്ടില്ല. [14] ഹെറിംഗ്-ബ്രൂവർ റിഫ്ലക്സ്, പൾമണറി സ്ട്രെച്ച് റിഫ്ലക്സ് എന്നിവയെ സൾഫർ ഡയോക്സൈഡ് തടയും.
തണുപ്പിക്കാനുള്ള ഉപയോഗം
[തിരുത്തുക]ഫ്രിയോണുകൾ കണ്ടുപിടിക്കുന്നതിനു മുൻപ് സൾഫർ ഡയോക്സൈഡ് റഫ്രിജിറേറ്ററുകളിൽ ഉപയോഗിച്ചിരുന്നു.
ലബോറട്ടറിയിൽ ലായകമായും മറ്റുമുള്ള ഉപയോഗം
[തിരുത്തുക]ഓക്സിഡൈസിംഗ് ലവണങ്ങളെ ലയിപ്പിക്കാനുള്ള ലായകമായി സൾഫർ ഡയോക്സൈഡ് ഉപയോഗിക്കാറുണ്ട്. സൾഫൊണൈൽ ഗ്രൂപ്പിന്റെ ഉത്പാദനത്തിനും ഇതുപയോഗിക്കും:[15]
അന്തരീക്ഷത്തിലെ മാലിന്യം
[തിരുത്തുക]
അഗ്നിപർവ്വതസ്ഫോടനങ്ങളിൽ നിന്ന് പുറത്തുവരുന്നതിനാലും മറ്റും അന്തരീക്ഷത്തിൽ സൾഫർ ഡയോക്സൈഡിന്റെ സാന്നിദ്ധ്യമുണ്ട്. [16] അമേരിക്കൻ ഐക്യനാടുകളിലെ പരിസ്ഥിതി സംരക്ഷണ ഏജൻസിയുടെ കണക്കനുസരിച്ച് [17]), താഴെപ്പറയുന്ന അളവ് സൾഫർ ഡയോക്സൈഡ് അമേരിക്കൻ ഐക്യനാടുകളിൽ പ്രതിവർഷം ബഹിർഗമിക്കുന്നുണ്ട്:
| വർഷം | SO2 (ആയിരം ഷോർട്ട് ടൺ വച്ച്) |
|---|---|
| 1970 | 31,161 |
| 1980 | 25,905 |
| 1990 | 23,678 |
| 1996 | 18,859 |
| 1997 | 19,363 |
| 1998 | 19,491 |
| 1999 | 18,867 |
മലിനീകാരി എന്ന നിലയിൽ മനുഷ്യാരോഗ്യത്തിൽ സൾഫർ ഡയോക്സൈഡ് വലിയ സ്വാധീനം ചെലുത്തുന്നുണ്ട്. [18] മൃഗങ്ങളെയും സസ്യങ്ങളെയും ഇത് ബാധിക്കും. [19]
കൽക്കരിയിൽ നിന്ന് സൾഫർ ഡയോക്സൈഡ് ഫ്ലൂയിഡൈസ്ഡ് ബെഡ് കംബഷൻ എന്ന പ്രക്രീയ ഉപയോഗിച്ച് നീക്കം ചെയ്യാൻ സാധിക്കും. [20] കത്തിക്കുന്നതിനു മുൻപ് ഇന്ധനങ്ങളിൽ നിന്ന് സൾഫർ നീക്കം ചെയതാൽ SO2 ഉണ്ടാകുന്നത് തടയാൻ സാധിക്കും. [21][22]
കാൽസ്യം, മഗ്നീഷ്യം ഓക്സൈഡ് എന്നിവ പെട്രോൾ, ഡീസൽ എഞ്ചിനുകളിൽ നിന്ന് സൾഫർ ഡയോക്സൈഡ് ഗാസ് ബഹിർഗമിക്കുന്നതു തടയാൻ കൂട്ടിച്ചേർക്കലിന് ഉപയോഗിക്കാറുണ്ട്. [23]
2006-ൽ ലോകത്തിൽ ഏറ്റവും കൂടുതൽ സൾഫർ ഡയോക്സൈഡ് പുറന്തള്ളുന്ന രാജ്യം ചൈനയായിരുന്നു[24]
സുരക്ഷ
[തിരുത്തുക]ശ്വസനം
[തിരുത്തുക]ഈ വാതകം ശ്വസിച്ചാൽ ശ്വാസകോശസംബന്ധമായ അസുഖലക്ഷണങ്ങൾ കാണപ്പെടും (ശ്വാസമെടുക്കാനുള്ള ബുദ്ധിമുട്ട് തുടങ്ങി മരണം വരെ സംഭവിക്കാം). [25] ശരാശരി 5 ppm (13 mg/m3) സുരക്ഷിതമായ അളവ്. [26]
സൾഫർ ഡയോക്സൈഡ് ശ്വസനവും വളർച്ചയെത്താതെ കുട്ടികൾ ജനിക്കുന്നതും തമ്മിൽ ബന്ധമുണ്ട്. [27]
ഉള്ളിലെത്തൽ
[തിരുത്തുക]അമേരിക്കൻ ഐക്യനാടുകളിൽ ഭക്ഷ്യസാധനങ്ങൾ സൂക്ഷിക്കാൻ സൾഫർ ഡയോക്സൈഡും സോഡിയം ബൈസൾഫൈറ്റും ഉപയോഗിക്കാനുള്ള അനുമതിയുണ്ട്. [28]
ഇവയും കാണുക
[തിരുത്തുക]അവലംബം
[തിരുത്തുക]- ↑ Sulfur dioxide Archived December 30, 2019, at the Wayback Machine., U.S. National Library of Medicine
- ↑ "Sulfur Dioxide". Archived from the original on 2023-09-24. Retrieved 2024-03-22., U.S. National Library of Medicine
- ↑ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (87th ed.). Boca Raton, FL: CRC Press. ISBN 0-8493-0487-3.
- ↑ "Hazardous Substances Data Bank".
- ↑ Miller, J.W. Jr.; Shah, P.N.; Yaws, C.L. (1976). "Correlation constants for chemical compounds". Chemical Engineering. 83 (25): 153–180. ISSN 0009-2460.
- ↑ "C&L Inventory".
- ↑ 7.0 7.1 7.2 "NIOSH Pocket Guide to Chemical Hazards #0575". National Institute for Occupational Safety and Health (NIOSH).
- ↑ 8.0 8.1 "Sulfur dioxide". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, ISBN 0-12-352651-5
- ↑ Shriver, Atkins. Inorganic Chemistry, Fifth Edition. W. H. Freeman and Company; New York, 2010; p. 414.
- ↑ Current EU approved additives and their E Numbers, The Food Standards Agency website.
- ↑ Sulphites in wine, MoreThanOrganic.com.
- ↑ Tchobanoglous, George (1979). Wastewater Engineering (3rd ed.). New York: McGraw Hill. ISBN 0-07-041677-X.
- ↑ Liu, D.; Jin, H; Tang, C; Du, J (2010). "Sulfur dioxide: a novel gaseous signal in the regulation of cardiovascular functions". Mini-Reviews in Medicinal Chemistry. 10 (11): 1039–1045. PMID 20540708. Archived from the original on 2013-04-26. Retrieved 2012-07-23.
- ↑ R. V. Hoffman (1990), "m-Trifluoromethylbenzenesulfonyl Chloride", Org. Synth.; Coll. Vol., 7: 508
{{citation}}: Missing or empty|title=(help) - ↑ Volcanic Gases and Their Effects Archived 2016-01-30 at the Wayback Machine.. Volcanoes.usgs.gov. Retrieved on 2011-10-31.
- ↑ National Trends in Sulfur Dioxide Levels, United States Environmental Protection Agency.
- ↑ "Sulfur Dioxide".
- ↑ C.Michael Hogan. 2010. Abiotic factor. Encyclopedia of Earth. eds Emily Monosson and C. Cleveland. National Council for Science and the Environment. Washington DC
- ↑ Lindeburg, Michael R. (2006). Mechanical Engineering Reference Manual for the PE Exam. Belmont, C.A.: Professional Publications, Inc. pp. 27–3. ISBN 978-1-59126-049-3.
- ↑ "Lo-Cat Process". Archived from the original on 2010-03-04. Retrieved 2012-07-23.
- ↑ Process screening analysis of alternative gas treating and sulfur removal for gasification. (December 2002) Report by SFA Pacific, Inc. prepared for U.S. Department of Energy (PDF) . Retrieved on 2011-10-31.
- ↑ Walter R. May Marine Emissions Abatement. SFA International, Inc., p. 6.
- ↑ China has its worst spell of acid rain, United Press International.
- ↑ Sulfur Dioxide U.S. Environmental Protection Agency
- ↑ "NIOSH Pocket Guide to Chemical Hazards".
- ↑ Shah PS, Balkhair T, Knowledge Synthesis Group on Determinants of Preterm/LBW Births (2011). "Air pollution and birth outcomes: a systematic review". Environ Int. 37 (2): 498–516. doi:10.1016/j.envint.2010.10.009. PMID 21112090.
{{cite journal}}: CS1 maint: multiple names: authors list (link) - ↑ "Center for Science in the Public Interest – Chemical Cuisine". Retrieved March 17, 2010.
പുറത്തേയ്ക്കുള്ള കണ്ണികൾ
[തിരുത്തുക]- അമേരിക്കൻ ഐക്യനാടുകളിലെ പരിസ്ഥിതി സംരക്ഷണ ഏജൻസിയുടെ സൾഫർ ഡയോക്സൈഡിനെപ്പറ്റിയുള്ള പേജ്
- ഇന്റർനാഷണൽ കെമിക്കൽ സേഫ്റ്റി കാർഡ് 0074
- IARC മോണോഗ്രാഫുകൾ. "സൾഫർ ഡയോക്സൈഡും ചില സൾഫൈറ്റുകളും, ബൈസൾഫൈറ്റുകളും മെറ്റാബൈസൾഫൈറ്റുകളും" v54. 1992. p131.
- NIOSH-ലെ കെമിക്കൽ ഹസാർഡുകളെപ്പറ്റിയുള്ള പോക്കറ്റ് ഗൈഡ്
- സൾഫർ ഡയോക്സൈഡ്, മോളിക്യൂൾ ഓഫ് ദി മന്ത്

