Titanborid
| Kristallstruktur | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
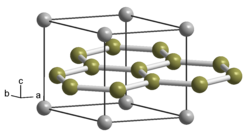
| |||||||||||||
| _ Ti _ B | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Titanborid | ||||||||||||
| Andere Namen |
Titandiborid | ||||||||||||
| Verhältnisformel | TiB2 | ||||||||||||
| Kurzbeschreibung |
graues Pulver[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 69,49 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Dichte |
4,52 g·cm−3 (25 °C)[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Titanborid, auch Titandiborid, ist eine anorganische chemische Verbindung des Bors aus der Gruppe der Boride.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Titanborid wird carbothermisch durch Sintern oder in flüssiger Phase im Lichtbogenofen dargestellt.[2] Es kann auch an glühenden Wolframfäden aus Dampfgemischen von Titan(III)-chlorid, Bortribromid und Wasserstoff bei 1400 bis 1600 °C gewonnen werden.[3]
Oder man setzt Gemische der flüchtigen Chloride mit Wasserstoff um:[4]
Es entsteht auch beim Sintern von Keramik mit ähnlichen Verbindungen.[5]
Auch die Herstellung durch Reaktion von Titandioxid mit Bortrioxid sowie Aluminium-, Silicium- oder Magnesiumpulver als Reduktionsmittel möglich.[6]
Beim sogenannten Borcarbidverfahren erfolgt eine Oberflächenhärtung zu Titanborid mit zusätzlichem Kohlenstoff und Titandioxid als Edukten:[6]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Titanborid ist ein graues Pulver,[1] das eine gute elektrische Leitfähigkeit besitzt.[2]
Verwendung
[Bearbeiten | Quelltext bearbeiten]Titanborid wird zusammen mit Bornitrid als Material für Verdampferschiffchen verwendet. In kleinerem Umfang wird es als Versuchsmaterial für Kathoden von Alumnium-Schmelzflusselektrolysezellen und als Panzermaterial[2][7] sowie als Ersatz für Diamantstaub und für Beschichtungen verwendet. Durch Einlagerung von Titanborid-Partikeln in Aluminium lassen sich die Eigenschaften (z. B. Härte) des Aluminiums verbessern, so nutzt man die »leichte« Legierung Al·x TiB2 anstelle schwerer Legierungen wie Stahl z. B. beim Fahrrad-, Motoren- und Flugzeugbau (nach ISPRAM-Verfahren = in situ processing of aluminum matrix composites).[8]
Es wird auch für Mantelrohre von Thermoelementen und zum Bau von Behältern für flüssige Metalle wie Aluminium eingesetzt.[9]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c d e f Datenblatt Titanium boride, powder, <10 μm bei Sigma-Aldrich, abgerufen am 15. September 2015 (PDF).
- ↑ a b c Wolfgang Kollenberg: Technische Keramik Grundlagen, Werkstoffe, Verfahrenstechnik. Vulkan-Verlag GmbH, 2004, ISBN 978-3-8027-2927-0, S. 339 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Richard Kieffer, Paul Schwarzkopf: Hartstoffe und Hartmetalle. Springer-Verlag, 2013, ISBN 978-3-7091-3901-1, S. 259 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Gert Blumenthal, Dietmar Linke, Siegfried Vieth: Chemie - Grundwissen für Ingenieure. Springer-Verlag, 2007, ISBN 978-3-8351-9047-4, S. 239 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Hermann Salmang, Horst Scholze: Keramik. Springer-Verlag, 2006, ISBN 978-3-540-49469-0, S. 380 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Horst Briehl: Chemie der Werkstoffe. Springer Science & Business Media, 2007, ISBN 978-3-8351-0223-1, S. 253 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ James W. McCauley, Andrew Crowson, William A. Gooch, Jr., A. M. Rajendran, Stephan J. Bless, Kathryn Logan, Michael Normandia, Steven Wax: Ceramic Armor Materials by Design. John Wiley & Sons, 2012, ISBN 1-118-38110-6, S. 633 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Nebengruppenelemente, Lanthanoide, Actinoide, Transactinoide Band 2: Nebengruppenelemente, Lanthanoide, Actinoide, Transactinoide, Anhänge. Walter de Gruyter GmbH & Co KG, 2016, ISBN 978-3-11-049590-4, S. 1806 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Ralf Steudel: Chemie der Nichtmetalle Synthesen - Strukturen - Bindung – Verwendung. Walter de Gruyter, 2013, ISBN 978-3-11-030797-9, S. 212 (eingeschränkte Vorschau in der Google-Buchsuche).





