Umbeliferon
| Umbeliferon | |
|---|---|
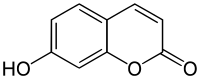 Strukturní vzorec | |
| Obecné | |
| Systematický název | 7-hydroxy-2H-1-benzopyran-2-on |
| Ostatní názvy | 7-hydroxykumarin, hydrangin, skimetin, beta-umbeliferon |
| Sumární vzorec | C9H6O3 |
| Vzhled | bílý až nažloutlý prášek[1] |
| Identifikace | |
| Registrační číslo CAS | 93-35-6 |
| EC-no (EINECS/ELINCS/NLP) | 202-240-3 |
| PubChem | 5281426 |
| ChEBI | 27510 |
| SMILES | C1=CC(=CC2=C1C=CC(=O)O2)O |
| InChI | InChI=1S/C9H6O3/c10-7-3-1-6-2-4-9(11)12-8(6)5-7/h1-5,10H |
| Vlastnosti | |
| Molární hmotnost | 162,14 g/mol |
| Teplota tání | 230,5 °C (503,6 K)[1] |
| Teplota varu | 382 °C (655 K)[1] |
| Hustota | g/cm3 |
| Rozpustnost ve vodě | rozpustný v horké vodě |
| Rozpustnost v polárních rozpouštědlech | dobře rozpustný v ethanolu |
| Bezpečnost | |
| [1] | |
| H-věty | H315 H319 H335[1] |
| P-věty | P261 P264 P264+265 P271 P280 P302+352 P304+340 P305+351+338 P319 P321 P332+317 P337+317 P362+364 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Umbeliferon, také nazývaný 7-hydroxykumarin, hydrangin, skimetin,, nebo beta-umbeliferon, je organická sloučenina patřící mezi kumariny.
Tato látka silně absorbuje ultrafialové záření na několika vlnových délkách. Existují náznaky jejích antimutagenních[2] a antioxidačních vlastností;[3][4] z těchto důvodů bývá přidávána do opalovacích krémů.[5]
Výskyt
[editovat | editovat zdroj]Umbeliferon se nachází v mnoha rostlinách z čeledi miříkovitých (Apiaceae nebo Umbelliferae), jako jsou mrkev, koriandr a andělika lékařská, ale i v jiných, například chlupáčku zedním (Hieracium pilosella, hvězdnicovité) nebo hortenzii velkolisté (Hydrangea macrophylla, hortenziovité, kde bývá nazýván hydranginem).
Tato látka je obsažena v pryskyřici rostliny nazývané čertovo lejno. Také se vyskytuje v druhu Justicia pectoralis.[6][7]
Biosyntéza
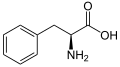
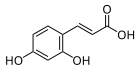
[editovat | editovat zdroj]Umbeliferon patří mezi fenylpropanoidy a výchozí látkou jeho syntézy je tak L-fenylalanin, vznikající v šikimátové dráze. Fenylalanin se působením fenylalaninamoniaklyázy přeměňuje na kyselinu skořicovou, která se následně hydroxylací pomocí cinamát-4-hydroxylázy mění na kyselinu 4-kumarovou. Tato kyselina je znovu hydroxylována, tentokrát cinamát/kumarát-2-hydroxylázou, na kyselinu umbelovou (2,4-dihydroxyskořicovou), u níž dojde k rotaci nenasycené vazby sousedící s karboxylovou skupinou. Nakonec způsobí vnitromolekulární reakce hydroxylové skupiny na C2' s karboxylovou uzavření kruhu a tvorbu laktonu umbeliferonu.
Umělá syntéza
[editovat | editovat zdroj]Umbeliferon se běžně připravuje Pechmannovou kondenzací resorcinolu s kyselinou formyloctovou (získanou z kyseliny jablečné).[8]
Byla vyvinuta novější příprava, založená na reakci methyl-propionátu za přítomnosti palladiového katalyzátoru.
Ultrafialová fluorescence
[editovat | editovat zdroj]Umbeliferon silně absorbuje na 300, 305 a 325 nm a fluoreskuje v ultrafialové oblasti i v modrém světle. Výrazná absorpce na třech vlnových délkách, ve spojení s vyzařováním energie ve viditelné, činí z umbeliferonu vhodnou přísadu do opalovacích krémů. Absorpce se mění v zásaditých roztocích, kde je fenolový hydroxyl deprotonován (pKa = 7,7).
Použití
[editovat | editovat zdroj]Pohlcování ultrafialového záření umbeliferonem má využití v opalovacích krémech a při optickém zjasňování textilií. Také se používá jako optické medium v barvivových laserech. Umbeliferon může být použit jako fluorescenční indikátor iontů kovů, jako jsou měď a vápník. Také může být indikátorem pH v rozmezí 6,5-8,9.
Umbeliferon působí jako inhibitor 17β-hydroxysteroiddehydrogenázy typu 3, enzymu zprostředkovávajícího přeměnu 4-androsten-3,17-dionu na testosteron.[9]
Deriváty
[editovat | editovat zdroj]Umbeliferon je základní strukturou několika přírodních látek. Herniarin (7-O-methylumbeliferon nebo 7-methoxykumarin) se vyskytuje v listech rostliny Ayapana triplinervis a v průtržnících (Herniaria). O-glykosylované deriváty, jako například skimin (7-O-β-D-glukopyranosylumbeliferon) se v přírodě také nacházejí a mají využití ve fluorimetrických určováních glykosidhydrolázových enzymů. K izoprenylovým derivátům patří mimo jiné marmin (ve slupkách grapefruitů a kůře oslizáku líbezného (Aegle marmelos) a furokumariny, například marmesin, angelicin a psoralen.
Umbeliferon-7-apiosylglukosid lze nalézt v kořenech rostliny Gmelina arborea.[10]
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Umbelliferone na anglické Wikipedii.
- ↑ a b c d e f https://pubchem.ncbi.nlm.nih.gov/compound/5281426
- ↑ T. Ohta; K. Watanabe; M. Moriya; Y. Shirasu; T. Kada. Anti-mutagenic effects of coumarin and umbelliferone on mutagenesis induced by 4-nitroquinoline 1-oxide or UV irradiation in e. Coli. Mutation Research. 1983, s. 135–138. Dostupné online. DOI 10.1016/0165-1218(83)90160-x. PMID 6403855.
- ↑ UMBELLIFERONE [online]. [cit. 2011-11-21]. Dostupné online.
- ↑ M. O. Sim; H. I. Lee; J. R. Ham; K. I. Seo; M. J. Kim; M. K. Lee. Anti-inflammatory and antioxidant effects of umbelliferone in chronic alcohol-fed rats. Nutrition Research and Practice. 2015, s. 364–369. DOI 10.4162/nrp.2015.9.4.364. PMID 26244074.
- ↑ Lupei Du. Rational design of a fluorescent hydrogen peroxide probe based on the umbelliferone fluorophore. Tetrahedron Letters. 2008, s. 3045–3048. DOI 10.1016/j.tetlet.2008.03.063. PMID 19081820.
- ↑ L. K. A. M. Leal; A. A. G. Ferreira; G. A. Bezerra; F. J. A. Matos; G. S. B. Viana. Antinociceptive, anti-inflammatory and bronchodilator activities of Brazilian medicinal plants containing coumarin: a comparative study. Journal of Ethnopharmacology. 2000, s. 151–159. DOI 10.1016/S0378-8741(99)00165-8. PMID 10771205.
- ↑ C. S. Lino; M. L. Taveira; G. S. B. Viana; F. J. A. Matos. Analgesic and antiinflammatory activities of Justicia pectoralis Jacq and its main constituents: coumarin and umbelliferone. Phytotherapy Research. 1997, s. 211–215. Dostupné online. DOI 10.1002/(SICI)1099-1573(199705)11:3<211::AID-PTR72>3.0.CO;2-W.
- ↑ V. K. Ahluwalia. Intermediates for Organic Synthesis. [s.l.]: I. K. International, 2010-09-30. ISBN 978-81-88237-33-3. S. 211.
- ↑ Donald Poirier. Inhibitors of 17 beta-hydroxysteroid dehydrogenases. Current Medicinal Chemistry. 2003, s. 453–477. DOI 10.2174/0929867033368222. PMID 12570693.
- ↑ P. Satyanarayana; P. Subrahmanyam; R. Kasai; O. Tanaka. An apiose-containing coumarin glycoside from gmelina arborea root. Phytochemistry. 1985, s. 1862–1863. DOI 10.1016/S0031-9422(00)82575-3.
Související články
[editovat | editovat zdroj]Literatura
[editovat | editovat zdroj]- DEAN, F.M. Naturally Occurring Oxygen Ring Compounds. London: Butterworths, 1963. Dostupné online. ISBN 978-0-408-26750-2.
- JOULE, J.A.; MILLS, K. Heterocyclic Chemistry. 4th. vyd. Oxford: Blackwell Science, 2000. ISBN 978-0-632-05453-4.
- Comprehensive Natural Products Chemistry. Redakce Barton D.H.R.. Oxford: Elsevier, 1999. ISBN 978-0-08-043154-3. S. 677.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Umbeliferon na Wikimedia Commons
Obrázky, zvuky či videa k tématu Umbeliferon na Wikimedia Commons - USDA ARS použití