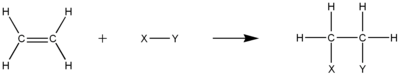Alken

Trong hóa hữu cơ, alken là một hydrocarbon chứa liên kết đôi carbon–carbon.[1] Alken thường đồng nghĩa với olefin. Thuật ngữ olefin dùng cho bất cứ hydrocarbon nào có chứa một hoặc nhiều liên kết đôi.[2] Tuy nhiên, Liên minh Hóa học Thuần túy và Ứng dụng Quốc tế (IUPAC) khuyến nghị chỉ sử dụng tên "alken" cho các hydrocarbon mạch hở chỉ có một liên kết đôi; alkadien, alkatrien, v.v., hoặc polyen đối với hydrocarbon mạch hở có hai hoặc nhiều liên kết đôi; cycloalken, cycloalkadien, v.v. đối với hợp chất vòng; và "olefin" cho hydrocarbon mạch vòng hay mạch hở có một hoặc nhiều liên kết đôi.[3][4][5]
Alken mạch hở, chỉ có 1 liên kết đôi và không chứa nhóm chức nào khác (còn gọi là alken đơn chức hay mono-en) tạo thành dãy đồng đẳng của hydrocarbon có công thức chung C
nH
2n với n từ 2 trở lên (ít hơn alkan tương ứng 2 hydro ). Khi n từ 4 trở lên thì có đồng phân dựa vào sự thay đổi vị trí nối đôi và vị trí các cấu phần liên kết với carbon có nối đôi.
Alken thường các hợp chất không phân cực không màu, hơi giống với alkan nhưng phản ứng mạnh hơn. Một số thành viên đầu tiên của chuỗi là chất khí hoặc chất lỏng ở nhiệt độ phòng. Alken đơn giản nhất, ethylen (C
2H
4) (danh pháp IUPAC: "ethen") là hợp chất hữu cơ được sản xuất ở quy mô công nghiệp lớn nhất.[6]
Các hợp chất thơm thường được gọi là alken vòng, tuy nhiên cấu trúc và tính chất của chúng đủ khác biệt để chất không được phân loại là alken hoặc olefin.[4] hydrocarbon có 2 liên kết đôi xen phủ (C=C=C ) được gọi là allen (hợp chất đơn giản nhất là allen) và những hợp chất có ba liên kết đôi liền nhau trở lên (C=C=C=C, C=C=C=C=C, v.v.) được gọi là cumulen.
Đồng phân cấu tạo
[sửa | sửa mã nguồn]Các alken có 4 nguyên tử carbon trở lên có thể tạo thành đồng phân cấu tạo. Hầu hết các alken là đồng phân của cycloalkan. Sau đây là số đồng phân cấu tạo của alken mạch hở có một liên kết đôi:[7]
- C
2H
4: ethylen - C
3H
6: propylen - C
4H
8: 3 đồng phân: 1-buten, 2-buten, and isobutylen - C
5H
10: 5 đồng phân: 1-penten, 2-penten, 2-methyl-1-buten, 3-methyl-1-buten, 2-methyl-2-buten - C
6H
12: 13 đồng phân: 1-hexen, 2-hexen, 3-hexen, 2-methyl-1-penten, 3-methyl-1-penten, 4-methyl-1-penten, 2-methyl-2-penten, 3-methyl-2-penten, 4-methyl-2-penten, 2,3-dimethyl-1-buten, 3,3-dimethyl-1-buten, 2,3-dimethyl-2-buten, 2-ethyl-1-buten - C
7H
14: 27 đồng phân (theo tính toán) - C
12H
24: 2,281 đồng phân (theo tính toán) - C
31H
62: 193,706,542,776 đồng phân (theo tính toán)
Nhiều phân tử trong số này có đồng phân cis–trans. Cũng có thể có các nguyên tử carbon bất đối đặc biệt trong các phân tử lớn (từ C
5 trở lên). Số lượng đồng phân tăng nhanh khi thêm tăng số nguyên tử carbon.
Cấu trúc và liên kết
[sửa | sửa mã nguồn]Liên kết
[sửa | sửa mã nguồn]
Liên kết đôi carbon-carbon cấu tạo bởi 1 liên kết sigma và 1 liên kết pi. Liên kết đôi này mạnh hơn liên kết đơn (C=C là 611 kJ / mol, còn C–C là 347 kJ/mol).[1] Liên kết đôi ngắn hơn liên kết đơn với độ dài liên kết trung bình là 1,33 Å (133 pm, C–C là 1,53 Å).
Mỗi nguyên tử carbon của liên kết đôi sử dụng ba orbital lai hóa sp2 để tạo thành liên kết sigma với ba nguyên tử khác. Các orbital nguyên tử 2p không lai hóa sẽ ở vị trí vuông góc với mặt phẳng tạo bởi trục của ba orbital lai hóa sp2, xen phủ nhau để tạo thành liên kết pi. Liên kết này nằm bên ngoài trục C–C chính, tạo liên kết pi có năng lượng liên kết yếu hơn đáng kể so với liên kết sigma, chỉ 65 kcal/mol.
Sự quay quanh liên kết đôi carbon-carbon bị hạn chế vì cần tiêu tốn năng lượng để phá vỡ liên kết của orbital p trên hai nguyên tử carbon. Do đó, sự chuyển đổi giữa đồng phân cis hoặc trans chậm đến mức có thể tách ra được dừng đồng phân riêng rẽ mà không bị đồng phân hóa. Các alken phức tạp hơn có thể được đặt tên bằng danh pháp E – Z cho các phân tử có 3 hoặc 4 nhóm thế khác nhau. Ví dụ, trong số các đồng phân của buten, hai nhóm methyl của (Z)-but-2-en (hay còn gọi là cis-2-buten) xuất hiện ở cùng một phía của liên kết đôi và trong (E)-but-2 -en (còn gọi là trans-2-buten), nhóm methyl xuất hiện ở hai phía đối diện. Hai đồng phân của buten có tính chất vật lý và hóa học riêng biệt.
Hình dạng
[sửa | sửa mã nguồn]Theo dự đoán của mô hình VSEPR về lực đẩy cặp electron, góc liên kết xung quanh mỗi nguyên tử carbon trong liên kết đôi khoảng 120°. Góc có thể thay đổi do tương tác Van der Waals được tạo ra bởi các tương tác không liên kết giữa các nhóm chức gắn với các nguyên tử carbon của liên kết đôi. Ví dụ, góc liên kết C–C–C trong propylen là 123,9°.
Đối với các alken có cầu nối, quy tắc Bredt phát biểu rằng liên kết đôi không thể xảy ra ở đầu cầu của hệ vòng có cầu nối, trừ khi các vòng đủ lớn.[8] Theo Fawcett định nghĩa: Lấy S là tổng số nguyên tử không nằm ở đầu cầu trong các vòng,[9] để ổn định cấu trúc phân tử, hệ hai vòng thì S ≥ 7[8] và hệ ba vòng thì S ≥ 11.[10]
Tính chất vật lý
[sửa | sửa mã nguồn]Nhiều tính chất vật lý của alken và alkan tương tự nhau: không màu, không phân cực và dễ cháy. Trạng thái vật lý phụ thuộc vào khối lượng phân tử: giống như các hydrocarbon no tương ứng, các alken đơn giản nhất (ethylen, propylen và buten) là chất khí ở nhiệt độ phòng. Các alken mạch thẳng có khoảng 5 đến 16 nguyên tử carbon ở thể lỏng và các alken có số carbon cao hơn là chất rắn dạng sáp. Nhiệt độ nóng chảy của chất rắn cũng tăng khi khối lượng phân tử tăng.
Các alken thường có mùi mạnh hơn các alkan tương ứng. Ethylen có mùi ngọt và giống như mùi mốc. Liên kết của ion cupric với olefin trong thụ thể khứu giác của động vật có vú (MOR244-3) có liên quan đến mùi của alken và thiol. Các alken mạch thẳng như norbornen và trans-cycloocten có mùi khó chịu, nồng.[11]
Tính chất hóa học
[sửa | sửa mã nguồn]Alken là hợp chất khá bền vững, nhưng dễ phản ứng hơn alkan. Phần lớn phản ứng của alken liên quan tới liên kết pi, để tạo thành liên kết đơn mới. Alken là nguyên liệu thô trong công nghiệp hóa dầu vì chúng tham gia nhiều vào các phản ứng hóa học như là polymer hóa và alkyl hóa
Ngoại trừ ethylen, các alken có hai vị trí phản ứng: liên kết pi carbon carbon và trung tâm CH allyl.
Phản ứng cộng
[sửa | sửa mã nguồn]Alken tham gia phản ứng cộng do có liên kết đôi. Hầu hết các phản ứng cộng này tuân theo cơ chế cộng electrophil, ví dụ: hydrohalogen hóa, halogen hóa, hình thành halohydrin, oxy-thủy ngân hóa, hydrobor-oxy hóa, cộng dichlorocarben, phản ứng Simmons–Smith, hydro hóa có xúc tác, epoxide hóa, phản ứng trùng hợp gốc và hydroxyl hóa.
Hydro hóa
[sửa | sửa mã nguồn]Hydro hóa alken tạo ra alkan tương ứng. Phản ứng đôi khi được thực hiện dưới áp suất và ở nhiệt độ cao. Chất xúc tác thường là kim loại. Các chất xúc tác công nghiệp chứa platin, nickel và paladi. Một ứng dụng quy mô lớn là sản xuất bơ thực vật.
Liên kết H−H hay tổng quát hơn là H−X sẽ phản ứng vào nối đôi. Phản ứng với H−X có ý nghĩa thương mại lớn. Một ví dụ là phản ứng cộng H-SiR3, tức là hydrosilyl hóa, để tạo ra các hợp chất cơ-silic. Một phản ứng khác là hydrocyanat hóa, chính là phản ứng cộng H−CN.
Hydrat hóa
[sửa | sửa mã nguồn]Hydrat hóa là cộng 1 phân tử nước vào liên kết đôi của alken, tạo ra alcohol. Phản ứng được xúc tác bởi acid phosphoric hoặc acid sulfuric. Phản ứng này được thực hiện ở quy mô công nghiệp để sản xuất ethanol tổng hợp.
Alken có thể biến đổi thành alcohol thông qua phản ứng oxy-thủy ngân hóa–de-thủy ngân hóa, phản ứng hydrobor hóa–oxy hóa hoặc bằng phản ứng hydrat hóa Mukaiyama.
Halogen hóa
[sửa | sửa mã nguồn]Trong phản ứng cộng halogen theo cơ chế electrophil, phản ứng cộng brom hoặc chlor vào alken tạo ra các dibromo- và dichloroalkan (hai nguyên tử trên ở vị trí carbon liền kề, tức là 1,2-dihalide hoặc ethylen dihalide). Nhận biết alken bằng phản ứng làm mất màu dung dịch nước brom.
Các phản ứng liên quan cũng được sử dụng làm thước đo định lượng độ bất bão hòa, được biểu thị bằng chỉ số brom và chỉ số iod của một hợp chất hoặc hỗn hợp.
Hydrohalogen hóa
[sửa | sửa mã nguồn]Hydrohalogen hóa là phản ứng cộng hydro halide, chẳng hạn như HCl hoặc HI, vào alken để tạo ra haloalkan tương ứng:
Nếu hai nguyên tử cacbon ở liên kết đôi liên kết với hydro có số lương nguyên tử khác nhau, thì halogen được ưu tiên cộng vào carbon có ít nhóm thế hydro hơn. Đây là quy tắc Markovnikov. Việc sử dụng các chất khơi mào gốc tự do có thể làm thay đổi kết quả sản phẩm. Đặc biệt là acid hydrobromic có xu hướng hình thành các gốc tự do khi có nhiều tạp chất hoặc thậm chí là oxy trong khí quyển, làm cho phản ứng không tuân theo quy tắc Markovnikov:[12]
Hình thành halohydrin
[sửa | sửa mã nguồn]Alken phản ứng với nước và halogen để tạo thành halohydrin bằng phản ứng cộng.
Oxy hóa
[sửa | sửa mã nguồn]Alken phản ứng với acid percarboxylic và thậm chí cả hydro peroxide để tạo ra epoxide:
Đối với ethylen, epoxy hóa được tiến hành trên quy mô công nghiệp bằng cách sử dụng oxy với sự có mặt của chất xúc tác:
Alken phản ứng với ozon, dẫn đến sự phân cắt của liên kết đôi. Phản ứng này được gọi là ozon phân. Thông thường, quy trình phản ứng thường có mặt chất khử nhẹ, chẳng hạn như dimethylsulfide (SMe
2):
Khi được xử lý bằng dung dịch acid hóa KMnO
4 đặc, nóng, alken bị phân cắt tạo thành keton và/hoặc acid carboxylic. Phản ứng này và ozon phân có thể được sử dụng để xác định vị trí của liên kết đôi trong một alken chưa biết.
Quá trình oxy hóa có thể dừng lại ở diol liền kề thay vì phân tách hoàn toàn alken bằng cách sử dụng osmi(VII) oxide hoặc các chất oxy hóa khác:
Phản ứng này được gọi là dihydroxyl hóa.
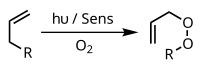
Với sự có mặt của chất nhạy quang thích hợp, chẳng hạn như xanh methylen và ánh sáng, các alken phản ứng với các gốc hydroxyl, oxy hoạt tính hoặc ion superoxide. Phản ứng có mặt chất nhạy có thể liên quan đến sự chuyền electron hoặc hydro, thường là với chất khử (phản ứng loại I) hoặc tương tác với oxy (phản ứng loại II).[13] Các phản ứng này có thể kiểm soát bằng cách lựa chọn các điều kiện phản ứng cụ thể, dẫn đến nhiều loại sản phẩm. Một ví dụ phổ biến là phản ứng cộng vòng [4+2] của oxy hoạt tính với một dien, chẳng hạn như cyclopentadien để tạo ra endoperoxide:
![Generation of singlet oxygen and its [4+2]-cycloaddition with cyclopentadiene](/media/wikipedia/commons/thumb/1/12/4%2B2_cycloaddition_cyclopentadiene_O2.svg/350px-4%2B2_cycloaddition_cyclopentadiene_O2.svg.png)
Một ví dụ khác là phản ứng ene, trong đó oxy hoạt tính phản ứng với cấu trúc allyl để tạo ra allyl peroxide chuyển vị:
Phản ứng trùng hợp (polymer hóa)
[sửa | sửa mã nguồn]Alken tận là tiền chất của polymer thông qua phản ứng trùng hợp. Một số phản ứng trùng hợp có ý nghĩa kinh tế lớn, vì chúng tạo ra nhựa polyethylen (PE) và polypropylen (PP). Polymer tạo thành từ alken thường được gọi là polyolefin mặc dù chúng không chứa olefin. Quá trình trùng hợp có thể tiến hành thông qua các cơ chế khác nhau. Dien liên hợp như buta-1,3-dien và isopren (2-methylbuta-1,3-dien, cấu tạo nên cao su tự nhiên) cũng tạo ra polymer.
Tạo phức kim loại
[sửa | sửa mã nguồn]
Cấu trúc của bis(cyclooctadien)nickel(0), một phức kim loại–alken
Alken là phối tử trong phức alken kim loại chuyển tiếp. Hai trung tâm carbon liên kết với kim loại bằng cách sử dụng orbital pi và pi* của C−C. Monolefin và diolefin thường được sử dụng làm phối tử trong các phức bền. Cyclooctadien và norbornadien là những tác nhân chelat phổ biến, và thậm chí bản thân ethylen còn được sử dụng làm phối tử trong muối Zeise. Ngoài ra, phức kim loại-alken là chất trung gian trong nhiều phản ứng xúc tác kim loại bao gồm hydro hóa, hydroformyl hóa và phản ứng trùng hợp.
Tổng hợp
[sửa | sửa mã nguồn]Phương pháp công nghiệp
[sửa | sửa mã nguồn]Alken được sản xuất bằng cách cracking hydrocacbon. Nguyên liệu chủ yếu là các thành phần khí tự nhiên ngưng tụ (chủ yếu là ethan và propan) ở Mỹ và Trung Đông và naphtha ở Châu Âu và Châu Á. Alkan bị phá vỡ ở nhiệt độ cao, thường có mặt chất xúc tác zeolit, để tạo ra hỗn hợp chủ yếu là alken béo và alkan có trọng lượng phân tử thấp hơn. Hỗn hợp này phụ thuộc vào nguyên liệu và nhiệt độ, và được phân tách bằng phương pháp chưng cất phân đoạn. Phương pháp trên chử yếu dùng để điều chế alken nhỏ (tối đa 6 nguyên tử carbon).[14]

Dehydro hóa có xúc tác là phản ứng trong đó một alkan tách hydro ở nhiệt độ cao để tạo ra alken tương ứng.[1] Đây là phản ứng ngược với phản ứng hydro hóa xúc tác của alken:
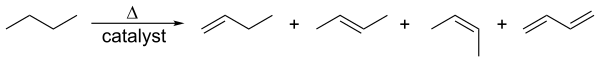
Quá trình này còn được gọi là reforming. Cả hai quá trình đều là quá trình thu nhiệt và sản phẩm thường là alken.
Các α-alken cao hơn (thuộc loại RCH=CH2) cũng có thể tổng hợp được dưới xúc tác bằng phản ứng của ethylen với hợp chất cơ kim triethyl nhôm (TEA), xúc tác nickel, cobalt hoặc platin.
Phản ứng tách
[sửa | sửa mã nguồn]Một trong những phương pháp chính để tổng hợp alken trong phòng thí nghiệm là dùng phản ứng tách các alkyl halide, alcohol và các hợp chất tương tự. Phổ biến nhất là tách β thông qua cơ chế phản ứng E2 (tách lưỡng phân tử) hoặc E1 (tách đơn phân tử),[15] nhưng cũng có thể tách α.
Cơ chế phản ứng tách lưỡng phân tử (E2) là cơ chế tách β tin cậy hơn so với cơ chế phản ứng tách đơn phân tử (E1) đối với hầu hết con đường tổng hợp alken. Hầu hết phản ứng tách E2 đều bắt đầu bằng alkyl halide hoặc ester alkyl sulfonat (chẳng hạn như tosylat hoặc triflat). Khi một alkyl halide được sử dụng, phản ứng được gọi là dehydrohalogen hóa. Đối với các chất bất đốt xứng, alken được hình thành với lượng lớn nhất là alken tách hydro từ carbon alpha (α-carbon) có ít nhóm thế là hydro nhất (xem quy tắc của Zaitsev). Hai phương pháp phổ biến của phản ứng tách là dehydrohalogen hóa của alkyl halide và phản ứng khử nước (dehydrat hóa) của alcohol. Ở ví dụ phía dưới, nếu H ở vị trí anti cũng có thể được tách ra, ngay cả khi sản phẩm tạo tách nếu tách H-anti tạo ra đồng phân Z kém bền hơn:[16]
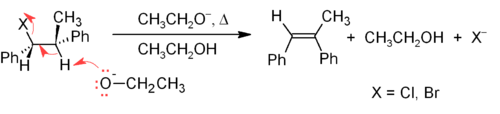
Alken có thể được tổng hợp từ alcohol thông qua phản ứng dehydrat hóa, trong trường hợp đó phân tử nước tách thông qua cơ chế E1. Ví dụ, quá trình khử nước của ethanol tạo ra ethylen:
- CH3CH2OH → H2C=CH2 + H2O
Alcohol có thể được chuyển hóa thành nhóm rời tốt hơn (ví dụ: xanthat), để cho phép cơ chế tách ở vị tri syn dễ hơn hơn như tách Chugaev và tách Grieco Các phản ứng liên quan: tách bằng β-haloether (tổng hợp Boord olefin) và ester (nhiệt phân ester).
Alken có thể được điều chế gián tiếp từ alkyl amin. Amin hoặc amonia không phải là nhóm rời thích hợp, do đó trước tiên, amin được alkyl hóa (như trong quá trình tách Hofmann ) hoặc bị oxy hóa thành amin oxide (phản ứng Cope) để có thể tách nhóm dễ dàng hơn. Phản ứng Cope tuân theo cơ thế tách-syn xảy ra ở khoảng nhiệt độ 150 °C, ví dụ:[17]
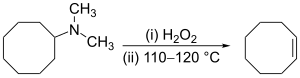
Tách Hofmann không bình thường ở chỗ các alken đi ngược lại quy tắc Zaitsev thường là sản phẩm chính.
Alken còn được tạo ra từ α-halosulfon trong phản ứng Ramberg–Bäcklund, thông qua một chất trung gian sulfon vòng ba cạnh.
Tổng hợp từ các hợp chất carbonyl
[sửa | sửa mã nguồn]Một phương pháp quan trọng khác để tổng hợp alken liên quan đến việc xây dựng liên kết đôi carbon-carbon mới bằng cách ghép hợp chất carbonyl (chẳng hạn như aldehyde hoặc keton) với một đương lượng carbanion. Những phản ứng như vậy đôi khi được gọi là phản ứng olefin hóa. Phương pháp nổi tiếng là phản ứng Wittig, nhưng các phương pháp liên quan khác cũng được biết đến như phản ứng Horner–Wadsworth–Emmons.
Phản ứng Wittig là phản ứng của aldehyde hoặc keton với thuốc thử Wittig (hoặc phosphoran) thuộc loại Ph3P=CHR để tạo ra alken và Ph3P=O (triphenylphosphin). Bản thân thuốc thử Wittig được điều chế dễ dàng từ triphenylphosphin với một alkyl halide. Phản ứng này khá chung chung và nhiều nhóm chức có thể phù hợp, thậm chí là ester, như trong ví dụ này:[18]
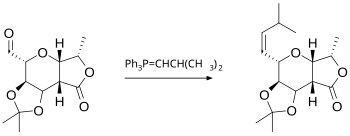
Liên quan đến phản ứng Wittig là phản ứng olefin hóa Peterson, sử dụng chất phản ứng dựa trên silic thay cho phosphoran. Phản ứng này cho phép tạo ra sản phẩm chọn lọc lập thể E- hoặc Z-. Nếu muốn có sản phẩm E, thì một giải pháp thay thế khác là phản ứng olefin hóa Julia, sử dụng carbanion được tạo ra từ phenyl sulfon. Phản ứng olefin hóa Takai dựa trên chất trung gian cơ-chromi cũng tạo ra các sản phẩm E-. Thuốc thử Tebbe là một hợp chất của titani rất hữu ích cho việc tổng hợp các hợp chất methylen; trong trường hợp này thậm chí ester và amide cũng tham gia phản ứng.
Một cặp ketone hoặc aldehyde có thể bị deoxygen hóa để tạo ra alken. Các alken đối xứng có thể được điều chế từ aldehyde hoặc keton phản ứng với chính nó, sử dụng quá trình khử kim loại titani (phản ứng McMurry). Nếu dùng các keton khác nhau trong phản ứng thì cần phải có một phương pháp phức tạp hơn, chẳng hạn như phản ứng Barton–Kellogg.
Một keton duy nhất cũng có thể được chuyển hóa thành alken tương ứng thông qua tosylhydrazon của nó, sử dụng natri methoxide (phản ứng Bamford–Stevens) hoặc alkyllithi (phản ứng Shapiro).
Tổng hợp từ alken
[sửa | sửa mã nguồn]Tổng hợp các alken dài hơn bằng phản ứng trùng hợp từng bước của các alken nhỏ hơn, vì ethylen (alken nhỏ nhất) vừa rẻ vừa sẵn có. Tổng hợp Ziegler–Natta cho phép hình thành các chuỗi rất dài như polyethylen. Khi muốn có các chuỗi ngắn hơn như trong sản xuất chất hoạt động bề mặt, có thể thể sử dụng các bước hoán vị olefin như quy trình olefin Shell.
Hoán vị olefin (olefin metathesis) được sử dụng trong thương mại nhằm chuyển hóa ethylen và 2-buten thành propylen. Hoán vị olefin mở ra con đường tổng hợp hữu cơ mới cho ngành hóa dầu, polymer và hóa chất đặc biệt quan trọng. Quá trình này sử dụng xúc tác dị thể chứa rheni và molybden:[19]
- CH2=CH2 + CH3CH=CHCH3 → 2 CH2=CHCH3
Hydrovinyl hóa xúc tác kim loại là một quá trình tổng hợp alken quan trọng khác có nguyên liệu ban đầu từ chính alken.[20] Phản ứng cộng một nhóm hydro và một nhóm vinyl (hoặc một nhóm alkenyl) vào liên kết đôi.
Từ alkyn
[sửa | sửa mã nguồn]Khử alkyn là một phương pháp hữu ích cho quá trình tổng hợp chọn lọc lập thể của các alken bất đối. Nếu muốn có cis-alken, thì phản ứng hydro hóa với sự có mặt của chất xúc tác Lindlar (một chất xúc tác dị thể chứa paladi lắng đọng trên calci carbonat và được xử lý bằng chì) thường được sử dụng. Khử alkyn bằng kim loại natri trong amonia lỏng sẽ cho ra sản phẩm dạng trans-alken.[21]
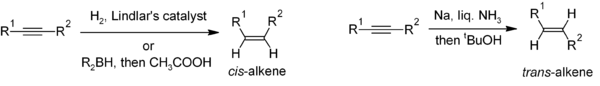
Để điều chế các alken nhiều vị trí bất đối xứng, carbometal hóa các alkyn có thể tạo ra nhiều loại dẫn xuất alken.
Chuyển vị và phản ứng liên quan
[sửa | sửa mã nguồn]Các alken có thể được tổng hợp từ các alken khác thông qua phản ứng chuyển vị. Bên cạnh hoán vị olefin (được mô tả ở trên), nhiều phản ứng pericyclic có thể được sử dụng như phản ứng ene và chuyển vị Cope.
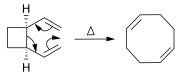
Trong phản ứng Diels–Alder, từ dien và alken có thể điều chế được cyclohexen.
Danh pháp IUPAC
[sửa | sửa mã nguồn]Mặc dù danh pháp IUPAC không được tuân theo rộng rãi, nhưng theo IUPAC, alken là một hydrocacbon mạch hở chỉ có một liên kết đôi giữa các nguyên tử carbon.[3] Olefin bao gồm một tập hợp lớn hơn các alken mạch vòng và mạch hở như dien và polyen.[4]
Danh pháp IUPAC cho các alken mạch thẳng, chỉ cần thay đổi hậu tố -an (của alkan) thành -en (của alken). Ví dụ, CH3-CH3 là alkan ethAN. Do đó, tên của CH2=CH2 là ethEN.
Đối với alken mạch thẳng có từ 4 nguyên tử carbon trở lên và các alken mạch hở phân nhánh, cần tuân theo quy tắc sau
- Tìm mạch carbon dài nhất trong phân tử. Nếu chuỗi đó không chứa liên kết đôi, hãy đặt tên cho hợp chất theo quy tắc đặt tên alkan. Nếu có chứa liên kết đôi thì:
- Đánh số các nguyên tử carbon trong chuỗi đó bắt đầu từ đầu gần với liên kết đôi nhất.
- Xác định vị trí của liên kết đôi, gọi vị trí này là k.
- Gọi tên các nhóm thế (ngoài hydro) theo quy tắc thích hợp.
- Xác định vị trí của mỗi nhóm thế là số thứ tự carbon trong mạch xác định từ bước 1 mà nhóm đó gắn vào.
- Viết vị trí và tên của mỗi nhóm thế.
- Viết tên các alkan cùng mạch, thay hậu tố "-an" bằng "k-en".
Theo IUPAC, cần viết số chỉ vị trí liên kết ở trước "en", ví dụ: "pent-2-en" thay vì "2-penten". Chú ý, nếu (H
3C)
3C–CH
2–CH
3 là "2,2-dimethyl pentane", thì (H
3C)
3C–CH=CH
2 là "3,3-dimethyl pen-1-ten".
Các quy tắc phức tạp hơn áp dụng cho polyen và cycloalken.[5]

Đồng phân cis–trans
[sửa | sửa mã nguồn]Nếu liên kết đôi của một mono-en mạch hở không phải là liên kết đầu tiên của chuỗi thì có thể sẽ có đồng phân cis – trans. Cần xác định xem hai liên kết C–C đơn liền kề với liên kết đôi nằm trên cùng một phía của mặt phẳng hay ở hai phía đối diện. Đối với monoalken, cấu hình thường được biểu thị bằng các tiền tố cis- (từ tiếng Latinh "ở bên này") hoặc trans- ("chéo", "ở bên kia") trước tên của hợp chất. Ví dụ: cis-pent-2-en hoặc trans-but-2-en.

Tổng quát hơn, đồng phân cis–trans sẽ tồn tại nếu mỗi nguyên tử cacbon trong liên kết đôi có hai nguyên tử hoặc nhóm khác nhau gắn vào nó. Tính đến những trường hợp này, IUPAC đề xuất danh pháp E–Z tổng quát hơn, thay vì các tiền tố cis và trans. Ký hiệu này xem xét nhóm có quy tắc ưu tiên Cahn–Ingold–Prelog cao nhất trong mỗi hai nguyên tử carbon. Nếu hai nhóm này nằm ở hai phía đối diện của mặt phẳng liên kết đôi, thì cấu hình được ký hiệu là E (từ tiếng Đức entgegen có nghĩa là "đối diện"); nếu chúng ở cùng một phía thì ký hiệu là Z (từ tiếng Đức zusammen, "cùng nhau"). " Để dễ nhớ hơn thì có mẹo nhớ như sau: Z trong cụm từ 'on ze zame zide', tức là cùng một phía.[22]

Nhóm chứa liên kết đôi C=C
[sửa | sửa mã nguồn]IUPAC công nhận hai tên cho các nhóm hydrocacbon chứa liên kết đôi carbon-carbon, nhóm vinyl và nhóm allyl.[5]

Xem thêm
[sửa | sửa mã nguồn]- Hydrocarbon thơm ("Aren")
- Nitroalken
Tham khảo cách gọi danh pháp hữu cơ
[sửa | sửa mã nguồn]- Rule A-3. Unsaturated Compounds and Univalent Radicals [1] IUPAC Blue Book.
- Rule A-4. Bivalent and Multivalent Radicals [2] IUPAC Blue Book.
- Rules A-11.3, A-11.4, A-11.5 Unsaturated monocyclic hydrocarbons and substituents [3] IUPAC Blue Book.
- Rule A-23. Hydrogenated Compounds of Fused Polycyclic Hydrocarbons [4] IUPAC Blue Book.
Tham khảo
[sửa | sửa mã nguồn]- ^ a b c Wade, L.G. (2006). Organic Chemistry (ấn bản thứ 6). Pearson Prentice Hall. tr. 279. ISBN 978-1-4058-5345-3.
- ^ H. Stephen Stoker (2015): General, Organic, and Biological Chemistry. 1232 pages. ISBN 9781305686182
- ^ a b IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "alkenes". doi:10.1351/goldbook.A00224
- ^ a b c IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "olefins". doi:10.1351/goldbook.O04281
- ^ a b c Moss, G. P.; Smith, P. A. S.; Tavernier, D. (1995). “Glossary of Class Names of Organic Compounds and Reactive Intermediates Based on Structure (IUPAC Recommendations 1995)”. Pure and Applied Chemistry. 67 (8–9): 1307–1375. doi:10.1351/pac199567081307.
- ^ “Production: Growth is the Norm”. Chemical and Engineering News. 84 (28): 59–236. 10 tháng 7 năm 2006. doi:10.1021/cen-v084n034.p059.
- ^ “Sloane's A000631”. Bảng tra cứu dãy số nguyên trực tuyến. Tổ chức OEIS.
- ^ a b Bansal, Raj K. (1998). “Bredt's Rule”. Organic Reaction Mechanisms (ấn bản thứ 3). McGraw-Hill Education. tr. 14–16. ISBN 978-0-07-462083-0.
- ^ Fawcett, Frank S. (1950). “Bredt's Rule of Double Bonds in Atomic-Bridged-Ring Structures”. Chem. Rev. 47 (2): 219–274. doi:10.1021/cr60147a003. PMID 24538877.
- ^ “Bredt's Rule”. Comprehensive Organic Name Reactions and Reagents. 116. 2010. tr. 525–528. doi:10.1002/9780470638859.conrr116. ISBN 978-0-470-63885-9.
- ^ Duan, Xufang; Block, Eric; Li, Zhen; Connelly, Timothy; Zhang, Jian; Huang, Zhimin; Su, Xubo; Pan, Yi; Wu, Lifang (28 tháng 2 năm 2012). “Crucial role of copper in detection of metal-coordinating odorants”. Proceedings of the National Academy of Sciences of the United States of America. 109 (9): 3492–3497. Bibcode:2012PNAS..109.3492D. doi:10.1073/pnas.1111297109. ISSN 0027-8424. PMC 3295281. PMID 22328155.
- ^ Streiwieser, A.; Heathcock, C.H.; Kosower, E.M. (1992). “11.6.G. Alkenes: Reactions: Free Radical Additions”. Introduction to Organic Chemistry (ấn bản thứ 4). New York: Macmillan. tr. 288.
- ^ Baptista, Maurício S.; Cadet, Jean; Mascio, Paolo Di; Ghogare, Ashwini A.; Greer, Alexander; Hamblin, Michael R.; Lorente, Carolina; Nunez, Silvia Cristina; Ribeiro, Martha Simões; Thomas, Andrés H.; Vignoni, Mariana (2017). “Type I and Type II Photosensitized Oxidation Reactions: Guidelines and Mechanistic Pathways”. Photochemistry and Photobiology. 93 (4): 912–919. doi:10.1111/php.12716. PMC 5500392. PMID 28084040.
- ^ Wade, L.G. (2006). Organic Chemistry (ấn bản thứ 6). Pearson Prentice Hall. tr. 309. ISBN 978-1-4058-5345-3.
- ^ Saunders, W. H. (1964). Patai, Saul (biên tập). The Chemistry of Alkenes. Wiley Interscience. tr. 149–150.
- ^ Cram, D.J.; Greene, Frederick D.; Depuy, C. H. (1956). “Studies in Stereochemistry. XXV. Eclipsing Effects in the E2 Reaction1”. Journal of the American Chemical Society. 78 (4): 790–796. doi:10.1021/ja01585a024.
- ^ Bach, R.D.; Andrzejewski, Denis; Dusold, Laurence R. (1973). “Mechanism of the Cope elimination”. J. Org. Chem. 38 (9): 1742–3. doi:10.1021/jo00949a029.
- ^ Snider, Barry B.; Matsuo, Y; Snider, BB (2006). “Synthesis of ent-Thallusin”. Org. Lett. 8 (10): 2123–6. doi:10.1021/ol0605777. PMC 2518398. PMID 16671797.
- ^ Lionel Delaude, Alfred F. Noels (2005). “Metathesis”. Kirk-Othmer Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH. tr. metanoel.a01. doi:10.1002/0471238961.metanoel.a01. ISBN 978-0471238966.
- ^ Vogt, D. (2010). “Cobalt-Catalyzed Asymmetric Hydrovinylation”. Angew. Chem. Int. Ed. 49 (40): 7166–8. doi:10.1002/anie.201003133. PMID 20672269.
- ^ Zweifel, George S.; Nantz, Michael H. (2007). Modern Organic Synthesis: An Introduction. New York: W. H. Freeman & Co. tr. 366. ISBN 978-0-7167-7266-8.
- ^ John E. McMurry (2014): Organic Chemistry with Biological Applications; 3rd edition. 1224 pages. ISBN 9781285842912