Benzofurano
| Benzofurano | |
|---|---|
 | |
 | |
 | |
| Nome IUPAC | |
| 1-benzofurano | |
| Nomi alternativi | |
| Benzo[b]furano Cumarone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C8H6O |
| Massa molecolare (u) | 118,13 |
| Aspetto | liquido incolore o giallo pallido |
| Numero CAS | |
| Numero EINECS | 205-982-6 |
| PubChem | 9223 |
| DrugBank | DBDB04179 |
| SMILES | C1=CC=C2C(=C1)C=CO2 |
| Proprietà chimico-fisiche | |
| Indice di rifrazione | 1,567 |
| Coefficiente di ripartizione 1-ottanolo/acqua | 2,670 |
| Temperatura di fusione | < -18 °C |
| Temperatura di ebollizione | 173-175 °C |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
 
| |
| attenzione | |
| Frasi H | 226 - 351 |
| Consigli P | 281 [1] |
Il benzofurano o cumarone, nome sistematico benzo[b]furano, è un composto organico eterociclico aromatico (biciclico), strutturalmente formato da un anello benzenico e uno di furano condensati. È l'analogo dell'indolo con l'ossigeno al posto dell'azoto.
Si presenta come un liquido incolore con punto di ebollizione di 173-175 °C, solubile in benzene, etere ed alcool. È un componente del catrame di carbon fossile, dal quale si può estrarre. Subisce reazioni di sostituzione elettrofila aromatica, quali alogenazioni e le reazioni di Friedel-Crafts.[2][3] Il benzofurano è alla base della struttura di molte sostanze organiche naturali e non. Lo psoralene, sostanza presente in parecchie piante, è un derivato del benzofurano.[4]
Produzione
[modifica | modifica wikitesto]È prodotto industrialmente per estrazione dal catrame di carbon fossile. È anche ottenuto per deidrogenazione del 2-etilfenolo.[5]
Sintesi di laboratorio
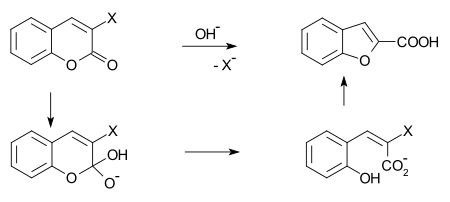
[modifica | modifica wikitesto]Il benzofurano può essere preparato per O-alchilazione della salicilaldeide con acido cloroacetico seguita da disidratazione (con ciclizzazione) dell'etere risultante, e poi decarbossilazione.[6] Una sintesi alternativa impiega il riarrangiamento di Perkin,[7][8] che comporta la reazione di una cumarina con uno ione idrossido:
Note
[modifica | modifica wikitesto]- ^ Sigma Aldrich; rev. del 23.12.2011
- ^ (EN) COUMARONE, in Organic Syntheses, vol. 46, 1966, pp. 28, DOI:10.15227/orgsyn.046.0028. URL consultato il 30 luglio 2023.
- ^ (EN) P. Cagniant e D. Cagniant, Recent Advances in the Chemistry of Benzo[b]furan and Its Derivatives. Part I: Occurrence and Synthesis, vol. 18, Academic Press, 1º gennaio 1975, pp. 337–482, DOI:10.1016/s0065-2725(08)60132-4. URL consultato il 30 luglio 2023.
- ^ (EN) Jean L. Lim e Robert S. Stern, PUVA, Elsevier, 1º gennaio 2005, pp. 569–571, DOI:10.1016/b0-12-369400-0/00815-2, ISBN 978-0-12-369400-3. URL consultato il 30 luglio 2023.
- ^ Gerd Collin, Hartmut Höke "Benzofurans" in Ullmann's Encyclopedia of Industrial Chemistry, 2007, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.l03_l01
- ^ Albert W. Burgstahler and Leonard R. Worden “Coumarone” Organic Syntheses, Collected Volume 5, p.251 (1973). [1] (PDF)
- ^ W. H. Perkin, J. Chem. Soc., 1870, 23, 368; 1871, 24, 37.
- ^ Reactions of carbonyl compounds in basic solutions. Part 32.1 The Perkin rearrangement Keith Bowden and Sinan Battah J. Chem. Soc., Perkin Trans. 2, 1998, 1603 - 1606, DOI: 10.1039/a801538d
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su benzofurano
Wikimedia Commons contiene immagini o altri file su benzofurano
| Controllo di autorità | Thesaurus BNCF 71610 · LCCN (EN) sh85013243 · GND (DE) 4144532-6 · J9U (EN, HE) 987007283132005171 · NDL (EN, JA) 00566979 |
|---|