Miastenia
| Myasthenia gravis pseudoparalytica | |
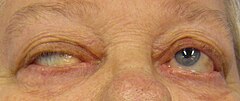 Opadanie powieki u osoby z miastenią | |
| Klasyfikacje | |
| ICD-10 | |
|---|---|
Miastenia (miastenia rzekomoporaźna, choroba Erba-Goldflama, łac. myasthenia gravis, ang. myasthenia gravis) – nabyta, przewlekła choroba, charakteryzująca się nużliwością (szybkim zmęczeniem i osłabieniem) mięśni szkieletowych. Przyczyną miastenii jest proces autoimmunologiczny, skierowany przeciwko receptorom acetylocholinowym.
Historia
[edytuj | edytuj kod]Pierwsze medyczne opisy miastenii pochodzą z XVII wieku. Chorobę opisywali Thomas Willis w 1672 i Samuel Wilks w 1877. Pod koniec XIX wieku poznano symptomatologię choroby, za sprawą prac Wilhelma Erba, Samuela Goldflama i Hermanna Oppenheima. Friedrich Jolly w 1895 wprowadził termin „Myasthenia gravis pseudoparalytica”. Związek miastenii z patologią grasicy odkrył Carl Weigert. Pierwszą tymektomię w terapii miastenii przeprowadził Ferdinand Sauerbruch w 1912. Próby farmakoterapii podjęła w latach 30. Mary Walker, sama chora na miastenię.
Epidemiologia
[edytuj | edytuj kod]Częstość choroby wynosi około 50–125:1 000 000. Kobiety chorują 2–3 razy częściej od mężczyzn. Dwie największe grupy chorych stanowią młode kobiety w wieku 20–35 lat i starsi mężczyźni w wieku 60–75 lat.
Etiologia
[edytuj | edytuj kod]Przyczyną miastenii jest autoimmunologiczny atak wyprodukowanych własnych przeciwciał skierowanych przeciwko receptorom dla acetylocholiny. Wynikiem tego jest spadek liczby receptorów w obrębie mięśni. Choroby grasicy, która nie uległa atrofii, współistnieją z miastenią. U około 10% pacjentów stwierdza się obecność guza nowotworowego grasicy – grasiczaka.
Objawy i przebieg
[edytuj | edytuj kod]Podstawowym objawem jest nadmierna męczliwość mięśni, manifestowana jako:
- opadanie powiek
- diplopia
- zmiana mimiki, tzw. uśmiech poprzeczny
- opadanie żuchwy
- osłabienie gryzienia, żucia, połykania pokarmów, nasilające się w miarę jedzenia
- osłabienie głosu, niewyraźna mowa w miarę wydawania głosu
- opadanie głowy
- osłabienie mięśni rąk w czasie wykonywania zwykłych czynności (mycie, czesanie, golenie się)
- osłabienie siły mięśni nóg przy chodzeniu
- upadki podczas biegu
- zaburzenia oddychania.
Kliniczny podział miastenii
[edytuj | edytuj kod]Zmodyfikowany podział Ossermana przedstawia się następująco:
- Grupa I – miastenia oczna
- Grupa IIA – łagodna miastenia uogólniona
- Grupa IIB – umiarkowana do ciężkiej miastenia uogólniona
- Grupa III – miastenia ostra (gwałtowna) lub ciężka uogólniona z niewydolnością oddechową
- Grupa IV – miastenia, późna, ciężka, ze znaczącą symptomatologią opuszkową.
Zazwyczaj opadanie powiek oraz podwójne widzenie pojawia się we wstępnej fazie choroby. Następna faza miastenii obejmuje mięśnie gardła i krtani, czego objawem jest „nosowy głos” oraz pojawiająca się dysfagia oraz trudności z żuciem pokarmów. Często zajmowane są również mięśnie tułowia i kończyn.
Besinger wprowadził system oceny punktowej objawów klinicznych oddający stopień ciężkości choroby. Składał się on z 8 objawów punktowanych od 0 do 3, gdzie 3 punkty oznaczały największe nasilenie objawu. Skalę tę rozszerzył Tindall do 13 objawów tworząc tzw. skalę QMG (Quantitative Myasthenia Gravis Test), używaną obecnie; najcięższa postać kliniczna miastenii określana jest w niej na 3x13=39 punktów[1].
Rozpoznanie
[edytuj | edytuj kod]Rozpoznanie opiera się o:
- wywiad
- stwierdzenie objawu apokamnozy, czyli wykazanie słabnięcia mięśni podczas pracy; np. przy osłabieniu mięśni opuszkowych poleca się pacjentowi liczenie do 50, przy obecnym objawie mowa staje się coraz bardziej nosowa i niewyraźna;
- dodatni wynik próby z chlorkiem edrofonium (Tensilonem): zmniejszeniu lub zniesieniu objawów po dożylnym podaniu 10 mg leku
- badania elektrofizjologiczne:
- stwierdzenie tzw. dekrementu miastenicznego w elektrostymulacyjnej próbie nużliwości
- ocena wyniku badania elektromiograficznego pojedynczego włókna mięśniowego (wydłużenie tzw. jittera).
- wykryciu przeciwciał anty-AChR i (lub) anty-MusK.
Różnicowanie
[edytuj | edytuj kod]W diagnostyce różnicowej miastenii rzekomoporaźnej należy uwzględnić:
- zespół miasteniczny Lamberta-Eatona
- botulizm
- zatrucie pestycydami
- zespół po leczeniu cuprenilem
- stwardnienie rozsiane
- guz pnia mózgu
- uszkodzenie nerwów gałkoruchowych
- miopatię oczno-gardłową
- miopatie mitochondrialne
- nerwicę
Leczenie
[edytuj | edytuj kod]Leczenie farmaceutyczne ma na celu zwiększenie stężenia acetylocholiny w złączach nerwowo-mięśniowych i zapobieganie wytwarzania przeciwciał receptorów acetylocholiny. W pierwszym celu stosuje się inhibitory cholinoesterazy:
Produkcję przeciwciał ogranicza się leczeniem immunosupresyjnym. Stosowane leki to:
Niekiedy stosuje się plazmaferezę i dożylne wlewy immunoglobulin. W razie wystąpienia niewielkich nawet objawów ze strony układu oddechowego, należy ocenić pojemność życiową płuc w badaniu spirometrycznym. Wartości poniżej 1,5 l są wskazaniem do przyjęcia pacjenta na oddział intensywnej opieki medycznej.
Leczenie chirurgiczne polega na usunięciu grasicy (tymektomia), do czego bezwzględnym wskazaniem jest podejrzenie grasiczaka. Usunięcie przerośniętej grasicy u pacjentów bez grasiczaka również, z niejasnych przyczyn, poprawia rokowanie.
W styczniu 2009 r. naukowcy z zespołu Henry’ego Kaminskiego z Saint Louis University opublikowali w Annals of Naurology artykuł, w którym twierdzą, że białko rEV756, znajdujące się w ślinie kleszczy i będące inhibitorem układu dopełniacza (białko to bowiem działa przez przyłączenie się do składnika C5 dopełniacza i zablokowanie jego interakcji z konwertazą C5 co blokuje powstawanie MAC – kompleksu atakującego błonę[2]) może grać znaczną rolę w leczeniu miastenii[2].
Rokowanie
[edytuj | edytuj kod]W miastenii jest bardzo zróżnicowane. U niektórych pacjentów dochodzi do samoistnej remisji. W przełomie miastenicznym złe, prowadzące do śmierci w wyniku zajęcia mięśni oddechowych.
Przypisy
[edytuj | edytuj kod]- ↑ R.J. Barohn, D McIntire, L Herbelin, GI Wolfe i inni. Reliability testing of the quantitative myasthenia gravis score. „Ann N Y Acad Sci”. 841, s. 769–772, 1998. PMID: 9668327.
- ↑ a b J. Soltys i inni, Novel complement inhibitor limits severity of experimentally myasthenia gravis, „Annals of Neurology”, 1, 65, 2009, s. 67–75, DOI: 10.1002/ana.21536 [dostęp 2010-11-17] (ang.).
Bibliografia
[edytuj | edytuj kod]- Miastenia i zespoły miasteniczne. W: Maria H. Strugalska-Cynowska: Neurologia. Podręcznik dla studentów medycyny. Wojciech Kozubski, Paweł P. Liberski (red.). Warszawa: Wydawnictwo Lekarskie PZWL, 2006, s. 324–334. ISBN 83-200-3244-X.
- Choroby wewnętrzne. Przyczyny, rozpoznanie i leczenie, tom II. Andrzej Szczeklik (red.). Wydawnictwo Medycyna Praktyczna, 2005. ISBN 83-7430-031-0.
- Juel VC, Massey JM. Myasthenia gravis. „Orphanet J Rare Dis”. 2, s. 44, 2008. DOI: 10.1186/1750-1172-2-44. PMID: 17986328.
